��Ŀ����
8����ͼ��ʵ�����о�DZˮͧ�й�����ϵ��Ӧ������װ��ͼ���г������ԣ���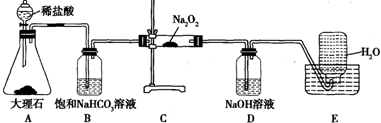
��1��Bװ�ÿɳ�ȥAװ���п��ܻӷ�����HCl����Ӧ�����ӷ���ʽΪHCO3-+H+�TH2O+CO2����
��2��Cװ��Ϊ02�ķ���װ�ã���Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2����
��3��Dװ�ÿɳ�ȥCװ����δ��Ӧ��CO2����Ӧ�����ӷ���ʽΪ2OH-+CO2�TCO32-+H2O��
��4��Cװ���й����ɵ���ɫ��ȫ��Ϊ��ɫ���������ɷֵ�ʵ�鷽��Ϊȡ����Cװ���з�Ӧ��Ĺ�������ˮ������Һ�е������CaCl2��BaCl2��Һ�����а�ɫ�������ɣ���֤�������к���Na2CO3�����ˣ�����Һ�е��뼸�η�̪��Һ������Һ����Ҳ���ɫ����֤�������к���NaOH��
���� ʵ�����о�DZˮͧ�й�����ϵ��Ӧ������Aװ�ã�ϡ����ʹ���ʯ��ȡ������̼��Bװ�ã��ñ��͵�̼�����Ƴ�ȥ������̼�е��Ȼ��⣬Cװ�ã�������̼��ˮ�ֱ�������Ʒ�Ӧ2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2����Dװ�ã���������������δ��Ӧ�Ķ�����̼��Eװ�ã�����ˮ���ռ��ƵõĶ�����̼��
��1��������лӷ��ԣ�ʯ��ʯ�����ᷴӦ�Ƿ��ȷ�Ӧ���������ɵĶ�����̼�к����Ȼ��⣬Ϊ����ȡ�����Ķ�����̼��Ӧ���ñ��͵�̼��������Һ��ȥ�Ȼ��⣻
��2��Cװ�ã�������̼��ˮ�ֱ�������Ʒ�Ӧ����������
��3��Dװ�ÿɳ�ȥCװ����δ��Ӧ�Ķ�����̼���������ƺ����������������κ�ˮ��
��4��Cװ���й����ɵ���ɫ��ȫ��Ϊ��ɫΪ̼����ƣ�����̼������Ӻ��Ȼ��������Ȼ�����Һ��Ӧ���ɻ�̼��ơ�̼�ᱵ��ɫ������֤̼������ӵĴ��ڣ����ˣ�����Һ�е��뼸�η�̪��Һ������Һ����Ҳ���ɫ����֤�������к��м
��� �⣺��1��Aװ�ã�ϡ����ʹ���ʯ��ȡ������̼������лӷ��ԣ�ʯ��ʯ�����ᷴӦ��CaCO3+2HCl=CaCl2+H2O+CO2�����÷�Ӧ�Ƿ��ȷ�Ӧ���������ɵĶ�����̼�к����Ȼ��⣬Ϊ����ȡ�����Ķ�����̼��Ӧ���ñ��͵�̼��������Һ��ȥ�Ȼ��⣬�Ȼ����̼�����Ʒ�Ӧ�����ɶ�����̼��������ȥ�Ȼ�������Ӷ�����̼������������̼��������Һ��ȥ�Ȼ��⣬��ӦΪ��HCO3-+H+�TH2O+CO2����
�ʴ�Ϊ��HCl�� HCO3-+H+�TH2O+CO2����
��2��Aװ���ƵõĶ�����̼�ܹ���������Ʒ�Ӧ������������ӦΪ��2Na2O2+2CO2�T2Na2CO3+O2����B�г��������庬��ˮ������ˮ�����ܹ���������Ʒ�Ӧ������������ӦΪ��2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2����
��3��Cװ�ã�������̼��ˮ�ֱ�������Ʒ�Ӧ��ͨ��Dװ����δ��Ӧ�Ķ�����̼���������ƺ����������������̼��Ӧ����̼���ƺ�ˮ����ӦΪ��2OH-+CO2�TCO32-++H2O��
�ʴ�Ϊ��CO2��2OH-+CO2�TCO32-++H2O��
��4��Cװ���й����ɵ���ɫNa2O2��ȫ��Ϊ��ɫΪ̼����ƣ���ӦΪ2Na2O2+2CO2�T2Na2CO3+O2���������ɷ�ʵ��Ϊ����̼������ӣ������Ȼ��������Ȼ�����Һ��̼������ӷ�Ӧ���ɻ�̼��ơ�̼�ᱵ��ɫ������֤̼������ӵĴ��ڣ����˳���������Һ�е��뼸�η�̪��Һ������Һ����Ҳ���ɫ����֤�������к����������ƣ�˵������2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��CaCl2��BaCl2��Na2CO3����Һ��죻NaOH��
���� ����Ϊ̽��������̼��ˮ��������Ʒ�Ӧʵ���⣬���ؿ�����ӡ�����ļ��飬��Ϥ��Ӧ��ԭ���ͳ�����������;�ǽ���ؼ�����Ŀ�Ѷ��еȣ�

| A�� | �����缫��Ϊ��Ƭ��M���������������Һ��0.4%��NaOH��Һ | |
| B�� | �����缫��Ϊʯī��M���������������Һ��0.4%��H2SO4��Һ | |
| C�� | �����缫��Ϊʯī��M���������������Һ��0.4%��KOH��Һ | |
| D�� | M����Ƭ����������N��ʯī���������Һ��0.4%��KNO3��Һ |
| A�� | 1000mL 50.0g | B�� | 950mL 47.5g | C�� | 950mL 30.4g | D�� | 1000mL 32.0g |
 �������һ�ֳ��õ��̬���ʣ����ҹ涨�����������£�
�������һ�ֳ��õ��̬���ʣ����ҹ涨�����������£�| ָ�� ��Ŀ | �ŵ�Ʒ | һ��Ʒ | �ϸ�Ʒ |
| �� �� | ��ɫ�ᾧ���ɼ���е���� | �ɼ���е���� | |
| ����N������ | ��21.0% | ��21.0% | ��20.5% |
[�۲����]������炙����ɼ���е���ʣ�
[ʵ����]
��1��ͨ��ʵ���Ҽ���ij��Ʒ�Ƿ�Ϊ��Σ��ǽ���Ʒ��B������ţ���ͬ�����ȣ�����C��E������������壮
A��ǿ�� B��ǿ��� C��ʪ��ĺ�ɫʯ����ֽD��ʪ�����ɫʯ����ֽ
E����պ��Ũ����IJ���������F����պ��Ũ����IJ�����
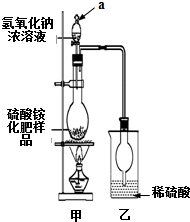
��2������ͼ��ʾװ�ý���ʵ�飮����a�������Ƿ�Һ©������ƿ�ڷ�����Ӧ�����ӷ���ʽΪ��NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
��3��ʵ������У�������ƿ�м�������Ũ����������Һ����ּ��ȣ�ԭ���ǣ�ʹ����麟�ַ�Ӧ��ȫת��ΪNH3����ȫ�������ձ��ң�
[��������]
��4��ijͬѧ���ݴ�ʵ���õ����ݣ���������炙��ʵĺ�����ƫ�ߣ���21.2%���������ʵ��װ���д���һ������ȱ���ǣ��ס���װ�ü�ȱһ������װ�ã�
[̽������]
��5���øĽ����ʵ��װ�����½���ʵ�飮��ȡ13.5g����炙�����Ʒ�����ʵ��ǰ����װ������3.40g���û��ʲ��ǣ���ǡ����ǡ���һ��Ʒ��
��2��2Ag��s��+$\frac{1}{2}$O2��g���TAg2O��s������H=-31.0kJ/mol
��ZnO��s��+2Ag��s���TZn��s��+Ag2O��s���ġ�H���ڣ�������
| A�� | -317.3kJ/mol | B�� | +317.3 kJ/mol | C�� | -379.3kJ/mol | D�� | -332.8kJ/mol |
| A�� | ʹ��̪�ʺ�ɫ����Һ��Na+��NH4+��Al3+��NO3- | |
| B�� | $\frac{{K}_{w}}{c��{H}^{+}��}$=0.1mol•L-1����Һ��Na+��K+��CO32-��ClO- | |
| C�� | ����Fe3+����Һ��Na+��Al3+��Cl-��SCN- | |
| D�� | ��ˮ���������c��OH-��=1��10-14mol•L-1��Һ��K+��Na+��Cl-��HCO3- |
 ��1�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ����Ӧ��O2��g����������H2O��g����ȥ����
��1�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ����Ӧ��O2��g����������H2O��g����ȥ���������д��������£�CH3OH��O2��Ӧ��Ҫ����HCHO�����CO��CO2����HCHO����
��2HCHO��g��+O2��g���T2CO��g��+2H2O��g����H=-470KJ•mol-1��
��2����֪��CO��g��+2H2��g��?CH3OH��g����H=-a kJ•mol-1��
���ⶨ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�������
| �¶ȣ��棩 | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |

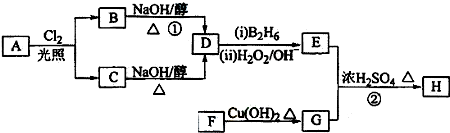
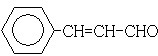 ��
�� ��
�� ��
�� ��
�� ��
�� �������������֣���
�������������֣���