题目内容
下列图示与对应的叙述相符的是( )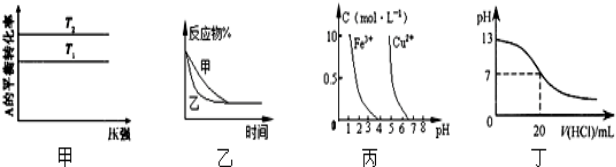

| A、图甲可以判断出反应A(g)+B(g)?2C(g)的△H<0,T2>T1 |
| B、图乙表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、依据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量的CuO,调节pH≈4 |
| D、图丁表示25℃时,用0.1 mol/L 盐酸滴定20 ml 0.1mol/LNaOH溶液,溶液的pH随加入盐酸体积的变化 |
考点:反应热和焓变,化学平衡的影响因素,难溶电解质的溶解平衡及沉淀转化的本质
专题:图示题
分析:A、给放热反应升高温度,平衡逆向移动;
B、反应前后气体体积不相等,加压平衡正向移动,不同压强下,平衡后反应物含量不相同;
C、pH=4时,铁离子水解完全铜离子还没有水解;
D、酸碱中和滴定时,有pH的突变过程.
B、反应前后气体体积不相等,加压平衡正向移动,不同压强下,平衡后反应物含量不相同;
C、pH=4时,铁离子水解完全铜离子还没有水解;
D、酸碱中和滴定时,有pH的突变过程.
解答:
解:A、给放热反应升高温度,平衡逆向移动,温度升高时,反应物转化率减小,故A错误;
B、正反应气体体积减小,加压平衡正向移动,乙比甲平衡时反应物百分含量降低,故B错误;
C、pH=4时,铁离子水解完全铜离子还没有水解,在溶液中加入CuO可以反应掉部分氢离子,增大溶液的pH,故C正确;
D、酸碱中和滴定时,有pH的突变过程,丁图中没有,故D错误;
故选C.
B、正反应气体体积减小,加压平衡正向移动,乙比甲平衡时反应物百分含量降低,故B错误;
C、pH=4时,铁离子水解完全铜离子还没有水解,在溶液中加入CuO可以反应掉部分氢离子,增大溶液的pH,故C正确;
D、酸碱中和滴定时,有pH的突变过程,丁图中没有,故D错误;
故选C.
点评:注意识图能力是解决问题的关键,考查学生对质的梳理和归纳能力,综合性较强,难度较大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、离子晶体中只存在离子键 |
| B、稀有气体形成的晶体属于分子晶体 |
| C、干冰升华时,分子内共价键会发生断裂 |
| D、由非金属元素形成的化合物一定是共价化合物 |
下列说法正确的是( )
| A、摩尔是物质的数量单位 |
| B、1mol H2含有6.02×1023个氢原子 |
| C、气体的体积随压强增大和温度降低而变小 |
| D、在标准状况下,任何物质的摩尔体积都约22.4L |
 X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图所示.X.Y.Z的最外层电子数之和为14,下列说法中正确的是( )
X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如图所示.X.Y.Z的最外层电子数之和为14,下列说法中正确的是( )| A、原子半径:W>Z>Y>X |
| B、W的单质能与水反应,生成一种具有漂白性的物质 |
| C、四种元素的氢化物中,Z的氢化物最稳定 |
| D、最高价氧化物对应水化物的酸性:W>Z>X |
 锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为101kPa,温度为0℃):
锌与不同浓度的硫酸反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图装置进行实验(实验时压强为101kPa,温度为0℃):