题目内容
下列说法正确的是( )
| A、摩尔是物质的数量单位 |
| B、1mol H2含有6.02×1023个氢原子 |
| C、气体的体积随压强增大和温度降低而变小 |
| D、在标准状况下,任何物质的摩尔体积都约22.4L |
考点:物质的量的单位--摩尔,气体摩尔体积,阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、摩尔是物质的量的单位;
B、H2是双原子分子;
C、气体的质量一定,则气体的物质的量一定,影响气体的体积因素有压强、温度.
D、1mol气态物质在标准状况下的体积为22.4L.
B、H2是双原子分子;
C、气体的质量一定,则气体的物质的量一定,影响气体的体积因素有压强、温度.
D、1mol气态物质在标准状况下的体积为22.4L.
解答:
解:A、摩尔是物质的量的单位,故A错误;
B、H2是双原子分子,故1molH2含2mol氢原子,个数为12.04×1023个,故B错误;
C、气体的质量一定,则气体的物质的量一定,根据pV=nRT可知,体积随压强增大和温度降低而变小,故C正确;
D、1mol气态物质在标准状况下的体积为22.4L,1mol液态、固态物质的体积小于22.4L,故D错误;
故选C.
B、H2是双原子分子,故1molH2含2mol氢原子,个数为12.04×1023个,故B错误;
C、气体的质量一定,则气体的物质的量一定,根据pV=nRT可知,体积随压强增大和温度降低而变小,故C正确;
D、1mol气态物质在标准状况下的体积为22.4L,1mol液态、固态物质的体积小于22.4L,故D错误;
故选C.
点评:本题考查了气体摩尔体积及物质的量的相关计算,为高考高频考点,注意n=
只适用于气态物质,标准状况下,Vm=22.4L/mol,题目难度不大.
| V |
| Vm |

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列变化过程中的能量变化与其它三个不相同的是( )
| A、生石灰与水混合 |
| B、天然气燃烧 |
| C、浓硫酸溶于水 |
| D、干冰气化 |
已知:一般溶液浓度越大密度越大,氨水等例外.则体积为vL、质量为mg,浓度为a mol/L的氨水溶液的溶质质量分数为b%,用水稀释到0.5a mol/L,下列说法正确的是( )
| A、加水的体积为vL |
| B、加水的质量为mg |
| C、0.5amol/L的氨水质量分数等于0.5b% |
| D、0.5amol/L的氨水质量分数小于0.5b% |
与250mL 0.4mol?L-1稀硫酸中的c(H+)相等的是( )
| A、100 mL 2 mol?L-1的盐酸溶液 |
| B、25 mL 0.8 mol?L-1的稀HNO3溶液 |
| C、100 mL 1 mol?L-1的稀H2SO4溶液 |
| D、250 mL 0.4 mol?L-1的稀盐酸溶液 |
在0.5L某浓度的Na2SO4溶液中含有0.5mol Na+,对该溶液的说法不正确的是( )
| A、该溶液的物质的量浓度为1 mol?L-1 |
| B、该溶液中含有35.5 g Na2SO4 |
| C、配制100 mL该溶液需用7.1 g Na2SO4 |
| D、量取100 mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1 mol |
浊液区别于其他分散系最本质的特征是( )
| A、外观混浊不清 |
| B、分散质粒子不能透过半透膜 |
| C、不稳定 |
| D、分散质粒子直径大于10-7m |
 如图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标,这里的钙、镁、钾、钠是指( )
如图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标,这里的钙、镁、钾、钠是指( )| A、元素 | B、原子 | C、单质 | D、分子 |
下列图示与对应的叙述相符的是( )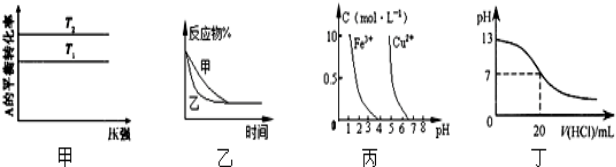

| A、图甲可以判断出反应A(g)+B(g)?2C(g)的△H<0,T2>T1 |
| B、图乙表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、依据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量的CuO,调节pH≈4 |
| D、图丁表示25℃时,用0.1 mol/L 盐酸滴定20 ml 0.1mol/LNaOH溶液,溶液的pH随加入盐酸体积的变化 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 | ||
B、c(OH-)=
| ||
| C、使石蕊试液呈紫色的溶液 | ||
| D、c(H+)=10-7mol/L的溶液 |