题目内容
下列说法正确的是( )
| A、离子晶体中只存在离子键 |
| B、稀有气体形成的晶体属于分子晶体 |
| C、干冰升华时,分子内共价键会发生断裂 |
| D、由非金属元素形成的化合物一定是共价化合物 |
考点:共价键的形成及共价键的主要类型,离子晶体,分子晶体
专题:
分析:A.含有离子键的晶体是离子晶体,离子晶体中可能含有共价键;
B.稀有气体形成的晶体中只存在共价键;
C.干冰升华时只破坏分子间作用力;
D.由非金属元素形成的化合物可能是离子化合物.
B.稀有气体形成的晶体中只存在共价键;
C.干冰升华时只破坏分子间作用力;
D.由非金属元素形成的化合物可能是离子化合物.
解答:
解:A.含有离子键的晶体是离子晶体,离子晶体中可能含有共价键,如KOH等,故A错误;
B.稀有气体形成的晶体中只存在共价键,是由分子构成的,所以属于分子晶体,故B正确;
C.干冰升华时只发生物理变化,所以只破坏分子间作用力不破坏化学键,但离子晶体熔融时破坏化学键,故C错误;
D.由非金属元素形成的化合物可能是离子化合物,如铵盐,故D错误;
故选B.
B.稀有气体形成的晶体中只存在共价键,是由分子构成的,所以属于分子晶体,故B正确;
C.干冰升华时只发生物理变化,所以只破坏分子间作用力不破坏化学键,但离子晶体熔融时破坏化学键,故C错误;
D.由非金属元素形成的化合物可能是离子化合物,如铵盐,故D错误;
故选B.
点评:本题考查化学键、化合物的关系,侧重考查基本基本、基本概念,明确物质中存在的化学键是解本题关键,注意规律中的异常现象,采用列举法解答,题目难度不大.

练习册系列答案
相关题目
金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性.下列关于钠的叙述中,不正确的是( )
| A、钠是银白色金属,熔点低,硬度小 |
| B、钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠 |
| C、钠不能从盐溶液中置换出相应的金属 |
| D、金属钠着火不能用水灭火 |
下列变化过程中的能量变化与其它三个不相同的是( )
| A、生石灰与水混合 |
| B、天然气燃烧 |
| C、浓硫酸溶于水 |
| D、干冰气化 |
已知M2O7x-+3S 2-+14H+=2M3++3S↓+7H2O,则M2O7x-中的M的化合价为( )
| A、+2价 | B、+3价 |
| C、+4价 | D、+6价 |
已知:一般溶液浓度越大密度越大,氨水等例外.则体积为vL、质量为mg,浓度为a mol/L的氨水溶液的溶质质量分数为b%,用水稀释到0.5a mol/L,下列说法正确的是( )
| A、加水的体积为vL |
| B、加水的质量为mg |
| C、0.5amol/L的氨水质量分数等于0.5b% |
| D、0.5amol/L的氨水质量分数小于0.5b% |
与250mL 0.4mol?L-1稀硫酸中的c(H+)相等的是( )
| A、100 mL 2 mol?L-1的盐酸溶液 |
| B、25 mL 0.8 mol?L-1的稀HNO3溶液 |
| C、100 mL 1 mol?L-1的稀H2SO4溶液 |
| D、250 mL 0.4 mol?L-1的稀盐酸溶液 |
下列图示与对应的叙述相符的是( )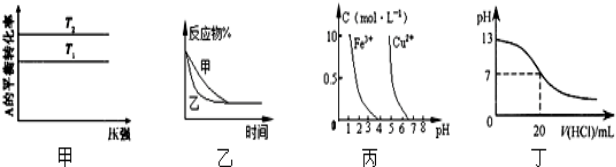

| A、图甲可以判断出反应A(g)+B(g)?2C(g)的△H<0,T2>T1 |
| B、图乙表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、依据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量的CuO,调节pH≈4 |
| D、图丁表示25℃时,用0.1 mol/L 盐酸滴定20 ml 0.1mol/LNaOH溶液,溶液的pH随加入盐酸体积的变化 |