题目内容
19.欲检验在制得的HCl气体中是否混有少量Cl2的方法是( )| A. | 用酚酞试纸 | B. | 用湿润的蓝色石蕊试纸 | ||
| C. | 用硝酸银溶液 | D. | 用湿润的淀粉-KI试纸 |
分析 氯气可与水反应生成具有漂白性的次氯酸,可用湿润的有色布条、淀粉碘化钾试纸检验.
解答 解:氯气、氯化氢都可与硝酸银反应生成白色沉淀,溶液都呈酸性,滴加酚酞不变色,不能检验,氯水具有氧化性,可与碘化钾生成碘,试纸变蓝色,加入蓝色石蕊试纸,因含有较少氯气,观察颜色为红色,不能检验,
故选D.
点评 本题考查物质的分离和提纯,为高频考点,侧重于学生的分析、实验能力的考查,题目难度不大,本题注意根据物质的性质的异同选择除杂方法,注意除杂时不能引入新的杂质.

练习册系列答案
相关题目
9.下列离子方程式书写正确的是( )
| A. | 将铝片插入硝酸铜溶液中:Cu2++Al=Al3++Cu | |
| B. | 盐酸与饱和的澄清石灰水反应:H++OH-══H2O | |
| C. | 碳酸钙与醋酸反应:CaCO3+2H+══Ca2++CO2↑+H2O | |
| D. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
10.已知25℃时,溶度积常数Ksp[Mg(OH)2]=1.8×10-11.在25℃时,0.1mol•L-1NH3•H2O溶液(该溶液中只有0.1%的NH3•H2O发生了电离)与pH=4的盐酸等体积混合后得到溶液M.则下列说法中错误的是( )
| A. | M溶液的pH>7 | |
| B. | 25℃时,溶度积常数Ka[NH3•H2O]约为1X10-7 | |
| C. | 25℃时,向M溶液中加少量盐酸,$\frac{c(N{H}_{4}^{+})}{(N{H}_{3}•{H}_{2}O)•c({H}^{+})}$的比值变小 | |
| D. | 25℃时,向1L0.2mol•L-1NH3•H2O溶液中加入1L0.2mol•L-1MgCl溶液,有Mg(OH)2沉淀产生(混合后溶液的体积变化不计) |
7.下列有关氯水的叙述,正确的是( )
| A. | 新制氯水只含有氯分子和次氯酸分子 | |
| B. | 新制氯水可使紫色石蕊试液先变红后褪色 | |
| C. | 氯水光照时有气泡逸出,该气体的主要成分是氯气 | |
| D. | 氯水放置数天后,其酸性逐渐减弱 |
14.下列离子方程式书写正确的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
4.下列与实验相关的叙述正确的是( )
| A. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| B. | 用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 | |
| C. | 用激光笔验证淀粉溶液的丁达尔现象 | |
| D. | 用洁净的玻璃棒蘸取碳酸钾溶液在酒精灯火焰上灼烧,可观察到明亮的紫色火焰 |
11.下列反应是非氧化还原反应的是( )
| A. | 2NO2+2NaOH═NaNO3+NaNO2+H2O | |
| B. | 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$ Fe3O4+4H2 | |
| C. | CaH2+2H2O═Ca(OH)2+2H2↑ | |
| D. | 3CCl4+K2Cr2O7═2CrO2Cl2+3COCl2+2KCl |
8.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 | |
| C. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| D. | 海水淡化的方法有蒸馏法、电渗析法等 |
9.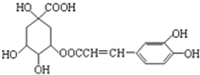 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,关于咖啡鞣酸的下列叙述正确的是( )
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,关于咖啡鞣酸的下列叙述正确的是( )
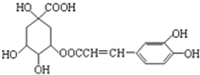 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,关于咖啡鞣酸的下列叙述正确的是( )
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示,关于咖啡鞣酸的下列叙述正确的是( )| A. | 分子式为C16H13O9 | |
| B. | 与浓溴水既能发生取代反应又能发生加成反应 | |
| C. | 1 mol咖啡鞣酸水解时可消耗8 mol NaOH | |
| D. | 能使酸性KMnO4溶液褪色,说明分子结构中有碳碳双键 |