题目内容
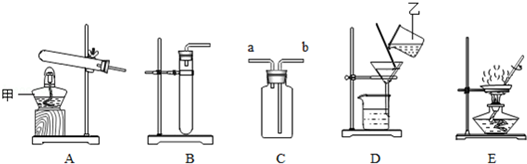
17. 某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )| A | B | C | D | |
| 纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
| 小烧坏中的溶液 | 浓氨水 | 浓氨水 | 氢氧化钠溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 由题干所给信息,滤纸折的蝴蝶喷上某种试剂后是白色的,说明该试剂是无色的,已知石蕊试液是紫色的,无色的酚酞溶液遇碱性溶液变红色,以及浓氨水呈碱性且有挥发性等知识点分析即可.
解答 解:从白色的蝴蝶变成红色可推断滤纸上喷洒的物质不是石蕊,而是酚酞试液;浓氨水有挥发性,挥发出的氨气遇到试剂中的水形成氨水,氨水呈碱性,无色的酚酞溶液遇碱性溶液变红色,氢氧化钠溶液没有挥发性,不能使蝴蝶变红.
故选B.
点评 本题考查了指示剂及元素化合物的性质,题目难度不大,注意根据题意运用排除法进行选择.

练习册系列答案
相关题目
7.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1.8 g D2O中含有的质子数、中子数均为NA | |
| B. | 标准状况下,22.4 L CCl4含有NA个CCl4分子 | |
| C. | 1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
8.下列有关热化学方程式的叙述中,正确的是( )
| A. | 含20.0gNaOH的稀溶液与足量稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(1)△H=-114.8kJ/mol | |
| B. | 已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ | |
| C. | 已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ/mol,则H2的燃烧热为241.8kJ/mol | |
| D. | 已知H+(aq)+OH-(aq)═H2O(1)△H=-57.31kJ•mol-1,故Ba2+(aq)+H+(aq)+OH-(aq)+SO42-(aq)═H2O(1)+BaSO4(s)△H<-57.31kJ•mol-1 |
12.关于下列各图的叙述,正确的是( )
| A. | 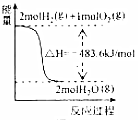 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ•mol-1 | |
| B. | 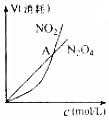 表示恒温恒容条件下发生的可逆反应2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 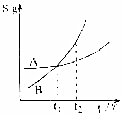 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数A=B | |
| D. | 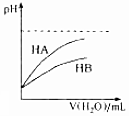 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
2. 向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )
向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )
 向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )
向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )| A. | a、d两点的沉淀为BaSO4 | B. | b、c两点溶液的导电能力相同 | ||
| C. | b、c两点溶液的PH值相同 | D. | d点溶液中大量存在的阳离子是K+ |
9.下列说法正确的是( )
| A. | pH均为2的醋酸和盐酸加水稀释100倍,所得溶液的pH:醋酸>盐酸 | |
| B. | pH为11的氨水和pH为3的盐酸溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol/L的NaOH溶液和CH3COONa溶液等体积混合后的溶液:c(Na+)+c(CH3COO-)=c(OH-)+c(H+) | |
| D. | 浓度均为0.1mol/L的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) |
6.已知四苯甲烷的结构式如图,下列有关它的说法中正确的是( )
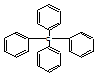

| A. | 它属于苯的同系物 | B. | 分子中所有原子共平面 | ||
| C. | 它的分子式为C25H24 | D. | 它的一氯代物有三种同分异构体 |