题目内容
6.已知四苯甲烷的结构式如图,下列有关它的说法中正确的是( )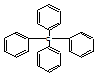
| A. | 它属于苯的同系物 | B. | 分子中所有原子共平面 | ||
| C. | 它的分子式为C25H24 | D. | 它的一氯代物有三种同分异构体 |
分析 分子中含有4个苯环,1个饱和碳原子,具有苯和甲烷的结构特点,结合有机物结构的对称性解答该题.
解答 解:A.含有4个苯环,与苯的结构不同,故A错误;
B.含有饱和碳原子,具有甲烷的结构特点,则分子中所有原子不可能共平面,故B错误;
C.由结构简式可知分子式为C25H20,故C错误;
D.四个苯环完全相同,每个苯环都有邻、间、对3种一氯代物,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的结构特点,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
17. 某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
 某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )| A | B | C | D | |
| 纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
| 小烧坏中的溶液 | 浓氨水 | 浓氨水 | 氢氧化钠溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
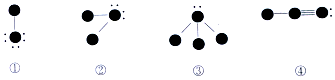
14.下列四种物质的结构图中,小黑球代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键,示例:如 ),下列说法正确的是( )
),下列说法正确的是( )
 ),下列说法正确的是( )
),下列说法正确的是( )
| A. | 四种物质中摩尔质量最大的是③ | B. | ①与③反应生成一种离子化合物 | ||
| C. | ④中含有非极性共价健 | D. | 该四种化合物涉及6种元素 |
1.实验室用浓盐酸与二氧化锰反应制取氯气,下列有关说法中正确的是(气体体积在.标况下测定)( )
| A. | 若提供0.4 mol HCl,MnO2过量,则可制得氯气4.48 L | |
| B. | 若提供0.4 mol HCl,MnO2过量,则转移电子数一定为0.1mol | |
| C. | 若有0.4 mol HCl参加反应,则可制得氯气2.24 L | |
| D. | 若有0.4 mol HCl被氧化,则可制得氯气2.24 L |
11.从防止污染和减少用酸量的角度分析,下列制取Cu(NO3)2的方法中最好的是( )
| A. | Cu$\stackrel{浓硝酸}{→}$Cu(NO3)2 | B. | Cu$\stackrel{稀硝酸}{→}$Cu(NO3)2 | ||
| C. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{硝酸}{→}$Cu(NO3)2 | D. | Cu$→_{△}^{浓硫酸}$CuSO4$\stackrel{硝酸钡}{→}$Cu(NO3)2 |
15.下列溶液中物质的量浓度关系正确的是( )
| A. | 室温,0.1mol•L-1的CH3COOH溶液中:c(CH3COOH)<c(CH3COO-) | |
| B. | 1L 0.1mol•L-1的(NH4)2Fe(SO4)2溶液中:c(SO${\;}_{4}^{2-}$)>c(NH${\;}_{4}^{+}$)>c(Fe2+)>c(H+)>c(OH-) | |
| C. | 室温,0.1mol•L-1的CH3COONa、NaOH和Na2CO3三种溶液,pH大小的顺序为:NaOH<CH3COONa<Na2CO3 | |
| D. | 向0.01mol•L-1的NaHSO4溶液中滴加NaOH溶液至中性时:c(SO${\;}_{4}^{2-}$)>c(Na+)>c(OH-)=c(H+) |