题目内容
7.设NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 1.8 g D2O中含有的质子数、中子数均为NA | |
| B. | 标准状况下,22.4 L CCl4含有NA个CCl4分子 | |
| C. | 1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
分析 A.重水的摩尔质量为20g/mol,1.8g重水的物质的量为0.09mol,重水中含有10个质子、10个电子;
B.气体摩尔体积使用对象为气体;
C.二价铁离子被过氧化氢氧化生成三价铁离子;
D.SO2和O2的反应是可逆反应,不能进行彻底.
解答 解:A.、1.8g重水的物质的量为0.09mol,0.09mol重水中含有0.9mol质子、0.9mol电子,含有的质子数和电子数均为0.9NA,故A错误;
B.标况下,四氯化碳为液态,不能使用气体摩尔体积,故B错误;
C.二价铁离子被过氧化氢氧化生成三价铁离子,1 mol Fe2+与足量的H2O2溶液反应,转移NA个电子,故C错误;
D.SO2和O2的反应是可逆反应,不能进行彻底,即不能彻底反应生成2molSO3,故混合气体的物质的量大于2mol,分子数大于2NA个,故D正确;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意气体摩尔体积使用条件和对象,注意可逆反应不能进行到底.

练习册系列答案
相关题目
18.某温度下硫酸铜的溶解度是25g,若温度不变,将32g无水硫酸铜粉末放入mg水中,形成饱和溶液并有胆矾晶体析出时,则m的取值范围是( )
| A. | 18g≤m≤128g | B. | 36g<m<180g | C. | 18g<m<128g | D. | 36g≤m≤128g |
15.一定温度下,两恒容容器中分别发生两个反应:①2X(g)+Y(g)?2Z(g);②A(g)+B(g)?C(g)+D(g),以下说法中,能说明反应①已经达到化学平衡状态、但不能说明反应②已经达到化学平衡状态的是( )
| A. | 反应容器中,气体物质的总质量不再变化 | |
| B. | 反应容器中,各物质的量不随时间变化 | |
| C. | 反应容器中,压强不随时间改变而改变 | |
| D. | 反应容器中,气体的密度不再改变 |
2.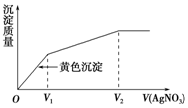 往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$的比值为( )
往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$的比值为( )
 往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$的比值为( )
往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.则原溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$的比值为( )| A. | V2-V1 | B. | $\frac{{V}_{1}}{{V}_{2}-{V}_{1}}$ | C. | $\frac{{V}_{1}}{{V}_{2}}$ | D. | $\frac{{V}_{2}}{{V}_{1}}$ |
19.常温时,将足量的AgCl分别加入下列各溶液中,AgCl的溶解度最小的是( )
| A. | 15mL 1.5 mol•L-1的AgNO3溶液 | B. | 10mL 2 mol•L-1的NaCl溶液 | ||
| C. | 5mL 1 mol•L-1的AlCl3溶液 | D. | 5mL 1.6mol•L-1的BaCl2溶液 |
17. 某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
 某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )
某学生用滤纸折成一只纸蝴蝶并在纸蝴蝶上喷洒某种试剂,挂在铁架台上.另取一只盛有某种溶液的烧杯,放在纸蝴蝶的下方(如图).过一会儿,发现白色纸蝴蝶上的喷洒液转变为红色,喷洒在纸蝴蝶上的试剂与小烧杯中的溶液是( )| A | B | C | D | |
| 纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
| 小烧坏中的溶液 | 浓氨水 | 浓氨水 | 氢氧化钠溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |