题目内容
17.已知某无色溶液中含有SO42-、Cl-、NO3-三种阴离子,则溶液中大量存在的阳离子是( )| A. | Ba2+ | B. | Fe3+ | C. | Ag+ | D. | Mg2+ |
分析 根据离子之间不能结合生成沉淀、气体、水等,则离子能大量共存,并结合离子的颜色来解答.
解答 解:A、硫酸根离子和钡离子结合产生硫酸钡沉淀,不能共存,故A错误;
B、铁离子能够和三种离子共存,但铁离子为黄色,不符合题意,故B错误;
C、银离子和氯离子结合产生氯化银沉淀,不能共存,故C错误;
D、镁离子和三种离子不能结合成沉淀、气体或水,能够共存,且不存在带色的离子,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,侧重于学生的分析能力的考查,熟悉复分解反应发生的条件即可解答,注意常见离子的颜色,题目难度不大.

练习册系列答案
相关题目
7.同温同压下,a g甲气体和2a g乙气体所占的体积之比为1:2,根据阿伏加德罗定律判断,下列叙述不正确的是( )
| A. | 同温同压下甲和乙的密度之比为1:1 | |
| B. | 等质量的甲和乙中的原子数之比为1:1 | |
| C. | 同温同体积下等质量的甲和乙的压强之比为1:1 | |
| D. | 甲与乙的相对分子质量之比为1:1 |
2.要降低过量Zn和一定量稀H2SO4间反应生成氢气速率,下列措施正确的是( )
| A. | 加入固体硫酸钠 | B. | 滴加几滴硫酸铜溶液 | ||
| C. | 升高稀硫酸温度 | D. | 加入硫酸钠溶液 |
12.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32-)>c(HCO3- )>c(OH-) | |
| B. | 20ml 0.1mol/L CH3COONa溶液与10ml 0.1mol/L HCl溶液混合后溶液呈酸性,所得溶液中:C(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+ )>c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
13.在下列各溶液中,离子一定能大量共存的是( )
| A. | 含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- | |
| B. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- | |
| C. | 加入铝粉有气泡产生的溶液中:Na+、NH4+、Fe2+、NO3- | |
| D. | 在AlCl3溶液中:K+、Na+、SiO32-、SO42- |

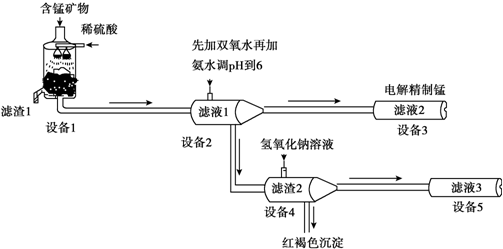
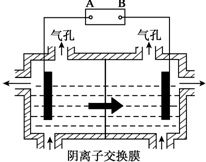 (5)设备3中用阴离子膜法提取金属锰的电解装置如图:
(5)设备3中用阴离子膜法提取金属锰的电解装置如图: