题目内容
18.设NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 在12 g单层石墨中,含六元环的数目为1NA | |
| B. | 50mL 18.4mol•L-1浓硫酸与足量铜加热充分反应,生成SO2分子的数目为0.46 NA | |
| C. | 42 g由乙烯和环丙烷组成的混合气体中,碳氢键的数目为6NA | |
| D. | 1mol过氧化钠与足量CO2充分反应,转移的电子数为2NA |
分析 A.每个碳原子被3个六元环公用,根据均摊法,一个六元环中含有的C原子数目为:1×$\frac{1}{3}$×6=2,12g石墨烯中含有1mol碳原子,能够形成0.5mol六元环;
B.铜只能与浓硫酸反应,随着反应进行,浓硫酸浓度降低,变为稀硫酸,不再与铜反应;
C.乙烯和环丙烷最简式相同为CH2,计算42gCH2中氢原子数,每个氢原子都连有一个C-H键;
D.过氧化钠与二氧化碳反应为歧化反应,1mol过氧化钠反应生成0.5mol氧气,转移1mol电子.
解答 解:A.12g石墨烯中含有12gC,含有1molC,每个六元环中含有2g碳原子,所以1molC原子可以形成0.5mol六元环,含六元环的个数为0.5NA,故A错误;
B.50mL 18.4mol/L的浓硫酸中H2SO4的物质的量=0.05L×18.4mol/L=0.92mol,若硫酸完全反应,由方程式可知生成二氧化碳的物质的量=0.92mol×12=0.46mol,由于Cu与浓硫酸反应,随反应进行,浓硫酸变稀,Cu不与稀硫酸反应,故实际得到SO2小于0.46mol,故B错误;
C.乙烯和环丙烷最简式相同为CH2,计算42gCH2中氢原子数=42g14g/mol×2×NA=6NA,含有碳氢键的数目为6NA,故C正确;
D.过氧化钠与二氧化碳反应为歧化反应,1mol过氧化钠反应生成0.5mol氧气,转移1mol电子,转移的电子数为NA,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意石墨烯的结构、铜与硫酸反应的条件、乙烯、环丙烷的结构,题目难度中等.

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
8.下列说法正确的是( )
| A. | CO2的比例模型为 | |
| B. | H2O2的电子式是H:O:O:H | |
| C. | 甲烷的结构式为CH4 | |
| D. | 熔融状态下NaHSO4的电离方程式为NaHSO4=Na++HSO4- |
9.胡妥油(D)用作香料的原料,它可由A合成得到:下列说法正确的是( )
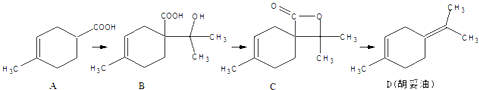

| A. | 若有机物A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的反应类型属于取代反应 | |
| B. | 有机物D分子中所有碳原子一定共面 | |
| C. | 有机物C的所有同分异构体中不可有芳香族化合物存在 | |
| D. | 有机物B既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体 |
6.工业上以粗盐为原料制取氢氧化钠时,首先要对粗盐进行除杂精制,为除去粗盐中的MgCl2、CaCl2、Na2SO4杂质,可加入氯化钡溶液、氢氧化钠溶液、碳酸钠溶液.则这三种试剂加入的顺序正确的是( )
| A. | 氢氧化钠溶液、碳酸钠溶液、氯化钡溶液 | |
| B. | 氢氧化钠溶液、氯化钡溶液、碳酸钠溶液 | |
| C. | 氯化钡溶液、碳酸钠溶液、氢氧化钠溶液 | |
| D. | 碳酸钠溶液、氯化钡溶液、氢氧化钠溶液 |
3.已知:二元酸H2R 的电离方程式是:H2R=H++HR-,HR-?R2-+H+,若0.1mol•L-1NaHR溶液的c(H+)=a mol•L-1,则0.1mol•L-1H2R溶液中c(H+)是( )
| A. | 小于 (0.1+a) mol•L-1 | B. | 大于 (0.1+a) mol•L-1 | ||
| C. | 等于 (0.1+a) mol•L-1 | D. | 等于2a mol•L-1 |
10.下列有关氨气或氨水的相关说法正确的是( )
| A. | 表面附着氨水的碳素钢在空气中主要发生析氢腐蚀 | |
| B. | 反应NH3(g)+HCl(g)?NH4Cl (s)的△H<0,△S<0 | |
| C. | 25℃时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液的pH>7 | |
| D. | 向2NH3(g)?N2(g)+3H2(g)的平衡体系中加入催化剂,NH3的平衡转化率增大 |