题目内容
10.下列有关氨气或氨水的相关说法正确的是( )| A. | 表面附着氨水的碳素钢在空气中主要发生析氢腐蚀 | |
| B. | 反应NH3(g)+HCl(g)?NH4Cl (s)的△H<0,△S<0 | |
| C. | 25℃时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液的pH>7 | |
| D. | 向2NH3(g)?N2(g)+3H2(g)的平衡体系中加入催化剂,NH3的平衡转化率增大 |
分析 A、氨水呈碱性,发生吸氧腐蚀;
B、反应NH3(g)+HCl(g)?NH4Cl (s)正反应是气体物质的量减少的放热反应,所以△H<0,△S<0;
C、25℃时,pH=11的氨水与pH=3的盐酸等体积混合,得到氨水和氯化铵的混合物以氨水的电离为主,溶液呈碱性;
D、使用催化剂平衡不移动.
解答 解:A、氨水呈碱性,发生吸氧腐蚀,而不是析氢腐蚀,故A错误;
B、反应NH3(g)+HCl(g)?NH4Cl (s)正反应是气体物质的量减少的放热反应,所以△H<0,△S<0,故正确;
C、25℃时,pH=11的氨水与pH=3的盐酸等体积混合,得到氨水和氯化铵的混合物以氨水的电离为主,溶液呈碱性,所以所得溶液的pH>7,故C正确;
D、使用催化剂平衡不移动,NH3的平衡转化率不变,故D错误;
故选BC.
点评 本题考查了电化腐蚀,平衡的移动,酸与碱混合后溶液pH的判断,其中A氨水呈碱性发生析氢腐蚀,题目难度中等.

练习册系列答案
相关题目
1.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 一定条件下,1 mol N2与足量H2反应生成NH3,转移电子6NA | |
| C. | 1L0.1 mol•L-1(NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
18.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 在12 g单层石墨中,含六元环的数目为1NA | |
| B. | 50mL 18.4mol•L-1浓硫酸与足量铜加热充分反应,生成SO2分子的数目为0.46 NA | |
| C. | 42 g由乙烯和环丙烷组成的混合气体中,碳氢键的数目为6NA | |
| D. | 1mol过氧化钠与足量CO2充分反应,转移的电子数为2NA |
5.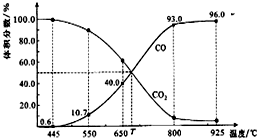 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )
 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如下图所示.下列说法正确的是( )| A. | 550℃时,若充入惰性气体,v正,?逆均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 该反应为放热反应 |
15.1mol•L-1的稀醋酸中存在平衡:CH3COOH?CH3COO-+H+.下列说法正确的是( )
| A. | 加水时,平衡向逆反应方向移动 | |
| B. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| C. | 加入少量0.1 mol•L-1盐酸,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
2.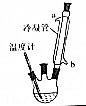 肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
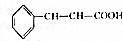 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$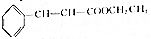 +H2O
+H2O
实验步骤:
制取:①在三颈烧瓶中加入20.0g肉桂酸、50.0g乙醇、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热至约75℃,回流12h.②进行蒸馏.③进行减压蒸馏,精制.最终制得17.6g肉桂酸乙酯.
(1)步骤①中冷凝管的作用是冷凝回流.
(2)步骤②中进行蒸馏的目的是除去乙醇,制备过程中需要控制温度在75℃,常采用的方法是水浴加热.
(3)本实验中加入过量乙醇的目的是提高肉桂酸的转化率.
(4)若要分离肉桂酸乙酯和水的混合物,常采用的分离方法是分液,分离过程中需要用到的玻璃仪器有分液漏斗.下图给出蒸馏操作中,仪器选择及安装都正确的是D(填字母序号).

(5)本实验中肉桂酸的利用率是74%.
 肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下:
肉桂酸乙酯具有草莓香味,用于配置香水、香精和人造精油.实验室制备肉桂酸乙酯的反应、装置示意图和有关数据如下: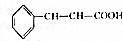 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$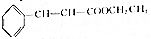 +H2O
+H2O | 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 乙醇 | 46 | 0.789 | 78.3 | 与水互溶 |
| 肉桂酸 | 148 | 1.245 | 300 | 微溶于水 |
| 肉桂酸乙酯 | 176 | 1.049 | 270 | 不溶于水 |
制取:①在三颈烧瓶中加入20.0g肉桂酸、50.0g乙醇、数滴浓硫酸和2~3片碎瓷片.开始缓慢加热至约75℃,回流12h.②进行蒸馏.③进行减压蒸馏,精制.最终制得17.6g肉桂酸乙酯.
(1)步骤①中冷凝管的作用是冷凝回流.
(2)步骤②中进行蒸馏的目的是除去乙醇,制备过程中需要控制温度在75℃,常采用的方法是水浴加热.
(3)本实验中加入过量乙醇的目的是提高肉桂酸的转化率.
(4)若要分离肉桂酸乙酯和水的混合物,常采用的分离方法是分液,分离过程中需要用到的玻璃仪器有分液漏斗.下图给出蒸馏操作中,仪器选择及安装都正确的是D(填字母序号).

(5)本实验中肉桂酸的利用率是74%.
1.短周期主族元素A、B、C、D、E的原子序数依次递增,A的单质在常温下呈气态,D元素的单质既能与盐酸反应也能与NaOH溶液反应,B、C、E原子的最外层电子数之和为13,E原子的最外层电子数是B原子内层电子数的3倍或是C原子最外层电子数的3倍.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(B)<r(C)<r(D) | |
| B. | 元素B、E的最高价氧化物的水化物都是强酸 | |
| C. | C、D的氧化物都能与氢氧化钠反应 | |
| D. | 工业上常用电解元素C、D的氯化物来制取它们的单质 |
2.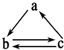 下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
 下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )
下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )| 物质 选项 | a | b | c |
| A | SiO2 | Na2SiO3 | H2SiO3 |
| B | C | CO | CO2 |
| C | Fe | FeCl2 | FeCl3 |
| D | CuO | Cu(OH)2 | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |