题目内容
9.胡妥油(D)用作香料的原料,它可由A合成得到:下列说法正确的是( )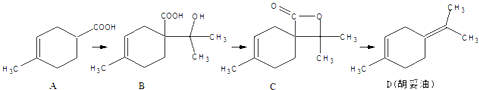
| A. | 若有机物A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的反应类型属于取代反应 | |
| B. | 有机物D分子中所有碳原子一定共面 | |
| C. | 有机物C的所有同分异构体中不可有芳香族化合物存在 | |
| D. | 有机物B既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体 |
分析 A.异戊二烯和丙烯酸发生加成反应生成有机物A;
B.有机物D中环状结构含3个亚甲基,为四面体结构;
C.有机物C中含碳碳双键、C=O键、2个环状结构;
D.有机物B含有羟基和羧基,羧基具有酸性.
解答 解:A.异戊二烯和丙烯酸发生类似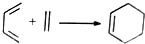 的加成反应生成有机物A,故A错误;
的加成反应生成有机物A,故A错误;
B.有机物D中环状结构含3个亚甲基,为四面体结构,则所以碳原子不会共面,故B错误;
C.有机物C中含碳碳双键、C=O键、2个环状结构,不饱和度为4,则可同分异构体中可能存在芳香族化合物,故C错误;
D.有机物B中含有羧基和羟基,都可与钠反应,其中羧基具有酸性,可与NaHCO3溶液反应放出CO2气体,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,题目难度中等,明确官能团与性质的关系为解答的关键,侧重烯烃、醇性质及同分异构体的考查,选项BC为易错点,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.用一种试剂除去下列各组物质中所含有的少量杂质(括号内为杂质),其中除杂方法正确的是( )
| A. | CO2(SO2):通过饱和Na2CO3溶液,洗气 | |
| B. | Cl2(HCl):通过NaOH固体,吸收 | |
| C. | BaCl2溶液(HCl):加入足量BaCO3,过滤 | |
| D. | FeCl3溶液(CuCl2):通入足量Fe,过滤 |
17.在一个密闭容器中发生如下反应:2SO2(g)+O2(g)?2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为:0.2mol•L-1、0.2mol•L-1、0.2mol•L-1,当反应达到平衡时,可能出现的数据是( )
| A. | c(SO3)=0.4 mol•L-1 | B. | c(SO2)=c(SO3)=0.15 mol•L-1 | ||
| C. | c(SO2)=0.25 mol•L-1 | D. | c(SO2)+c(SO3)=0.5 mol•L-1 |
4.在下面的反应中,氨作为氧化剂参加反应的是( )
| A. | NH3+H3PO4═NH4H2PO4 | |
| B. | 4NH3+5O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$4NO+6H2O | |
| C. | 2NH3+3Cl2═6HCl+N2 | |
| D. | NH3+NaH═NaNH2+H2↑ |
14.随着人们生活节奏的加快,方便的小包装食品已被广泛接受.为了延长食品的保质期,防止食品受潮变质,在包装袋中可以放入的化学物质是( )
| A. | 硅胶 | B. | 硫酸亚铁 | C. | 食盐 | D. | 石灰石 |
1.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 一定条件下,1 mol N2与足量H2反应生成NH3,转移电子6NA | |
| C. | 1L0.1 mol•L-1(NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
18.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 在12 g单层石墨中,含六元环的数目为1NA | |
| B. | 50mL 18.4mol•L-1浓硫酸与足量铜加热充分反应,生成SO2分子的数目为0.46 NA | |
| C. | 42 g由乙烯和环丙烷组成的混合气体中,碳氢键的数目为6NA | |
| D. | 1mol过氧化钠与足量CO2充分反应,转移的电子数为2NA |
1.短周期主族元素A、B、C、D、E的原子序数依次递增,A的单质在常温下呈气态,D元素的单质既能与盐酸反应也能与NaOH溶液反应,B、C、E原子的最外层电子数之和为13,E原子的最外层电子数是B原子内层电子数的3倍或是C原子最外层电子数的3倍.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(B)<r(C)<r(D) | |
| B. | 元素B、E的最高价氧化物的水化物都是强酸 | |
| C. | C、D的氧化物都能与氢氧化钠反应 | |
| D. | 工业上常用电解元素C、D的氯化物来制取它们的单质 |