题目内容
7.运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为5KClO3+6P=3P2O5+5KCl.下列有关该反应的叙述不正确的是( )| A. | KClO3是氧化剂 | B. | P2O5是氧化产物 | ||
| C. | 1molKClO3参加反应有6mole-转移 | D. | 每有6molP被还原,生成5molKCl |
分析 5KClO3+6P═3P2O5+5KCl中,Cl元素的化合价由+5价降低为-1价,则KClO3是氧化剂,P元素的化合价由0升高为+5价,则P是还原剂,生成P2O5是氧化产物,以此来解答.
解答 解:A.5KClO3+6P═3P2O5+5KCl中,Cl元素的化合价由+5价降低为-1价,则KClO3是氧化剂,故A正确;
B.P元素的化合价由0升高为+5价,则P是还原剂,生成P2O5是氧化产物,故B正确;
C.Cl元素的化合价由+5价降低为-1价,则1molKClO3参加反应有6mole-转移,故C正确;
D.P元素的化合价由0升高为+5价,P是还原剂被氧化,则每有6molP被氧化,生成5molKCl,故D错误;
故选D.
点评 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
14.下列关于常见物质的工业制法的叙述,不正确的是( )
| A. | 工业制硅:用焦炭在高温下还原二氧化硅可制得高纯硅 | |
| B. | 工业冶炼铁:需要用到的原料有铁矿石、焦炭、空气和石灰石 | |
| C. | 工业冶炼镁:电解熔融的无水氯化镁,可以得到金属镁 | |
| D. | 工业制玻璃:将石灰石、纯碱、石英在玻璃熔炉中高温熔融制得 |
18.把6moLM和5moLN的混合气体通入容积为4L的密闭容器中,在一定条件下发生如下反应:5M(g)+4N(g)?6P(g)+xQ(g),经5min后反应达到平衡,此时生成P 3moL,并测得Q的平均反应速率为0.1mol/(L•min)下列说法正确的是( )
| A. | 化学计量数x=2 | B. | M的转化率为41.67% | ||
| C. | N的平衡浓度为0.075mol/L | D. | 反应前后混合气体的压强比为$\frac{23}{22}$ |
15.下列物质在生活中有广泛应用,其中不属于离子化合物的是( )
| A. | NO | B. | Ca(ClO)2 | C. | NaCl | D. | NaHCO3 |
2.在向盛有氯化铁溶液的烧杯中加入过量铜粉,反应结束后过滤,对溶液中大量存在的金属阳离子的成分判断正确的是( )
| A. | 只有Cu2+ | B. | Fe2+、Cu2+ | C. | Fe3+、Fe2+ | D. | Fe3+、Cu2+ |
19.25°C时,水溶液中c(H+)与c(OH-)的变化关系如图中曲线 ac所示,下列判断错误的是( )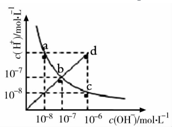

| A. | ac曲线上的任意一点都有c(H+)×c(OH-)=10-14 | |
| B. | CH3COONa溶液不可能位于c点 | |
| C. | d点对应溶液的温度高于25°C,PH<7 | |
| D. | bd线段上任意一点对应的溶液都呈中性 |
16.下列化学方程式书写正确的是( )
| A. | nCH2=CH2$\stackrel{催化剂}{→}$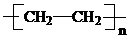 | |
| B. | CH2=CH2+Br2→CH3CHBr2 | |
| C. | 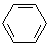 +HNO3$→_{60℃}^{浓硫酸}$ +HNO3$→_{60℃}^{浓硫酸}$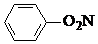 +H2O +H2O | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH3CH2+H2O |
17.下列关于有机化合物的说法正确的是( )
| A. | 2-甲基丁烷也称异丁烷 | |
| B. | 乙烯、苯都能发生加成反应 | |
| C. | 乙烯、聚氯乙烯分子中都含有碳碳双键 | |
| D. | 淀粉、油脂、蛋白质都属于高分子化合物 |
 A~H为中学化学中几种常见物质,它们之间的转化关系如图所示.常温下,A和G均为单质气体,同体C常用作干燥剂,E为无色、无味的液体,F为淡黄色粉末.回答下列问题:
A~H为中学化学中几种常见物质,它们之间的转化关系如图所示.常温下,A和G均为单质气体,同体C常用作干燥剂,E为无色、无味的液体,F为淡黄色粉末.回答下列问题: