题目内容
17.下列关于有机化合物的说法正确的是( )| A. | 2-甲基丁烷也称异丁烷 | |
| B. | 乙烯、苯都能发生加成反应 | |
| C. | 乙烯、聚氯乙烯分子中都含有碳碳双键 | |
| D. | 淀粉、油脂、蛋白质都属于高分子化合物 |
分析 A.2-甲基丁烷含5个C原子;
B.乙烯含碳碳双键,苯环为不饱和烃;
C.聚氯乙烯不含碳碳双键;
D.相对分子质量在10000以上的为高分子.
解答 解:A.2-甲基丁烷含5个C原子,则2-甲基丁烷也称异戊烷,故A错误;
B.乙烯含碳碳双键,苯环为不饱和烃,均可与氢气发生加成反应,分别生成乙烷、环己烷,故B正确;
C.聚氯乙烯不含碳碳双键,而乙烯含碳碳双键,故C错误;
D.淀粉、蛋白质都属于高分子化合物,而油脂不是,故D错误;
故选B.
点评 本题考查有机物的结构,为高频考点,把握有机物的组成、结构、官能团为解答的关键,侧重分析与应用能力的考查,注意常见的高分子化合物,题目难度不大.

练习册系列答案
相关题目
7.运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为5KClO3+6P=3P2O5+5KCl.下列有关该反应的叙述不正确的是( )
| A. | KClO3是氧化剂 | B. | P2O5是氧化产物 | ||
| C. | 1molKClO3参加反应有6mole-转移 | D. | 每有6molP被还原,生成5molKCl |
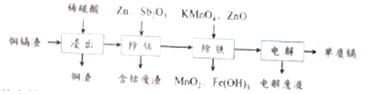
8.利用湿法炼锌产生的铜镉渣生产金属镉的流程如图:已知铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质.
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
(1)为了提高铜镉渣浸出的速率,可采取的措施有:①适当升高温度;②搅拌;③等.已知浸出的金属离子均为二价,写出浸出钴的化学方程式Co+H2SO4=CoSO4+H2↑
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3等形成微电池产生合金CoSb.该微电池的正极反应式为Sb2O3+Co2++6H++10e-=2CoSb+3H2O
(3)除铁的过程分两步进行,①加入适量KMnO4,发生反应的离子方程式为3Fe2++MnO4-+4H+=3Fe3++MnO2+2H2O,②加入ZnO控制反应液的PH范围为3.3-7.2
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是,若加入的KMnO4不足量,则待电解溶液中有Fe元残余.请设计实验方案加以验证.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Kap(CdCO3)=5.2×10-12
Kap(CdS)=3.6×10-29
Kap(Cd(OH)2)=2.0×10-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是b
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳PH为11,此时溶液中c(Cd2+)=2.0×10-10 mol•L-1.

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1mol•L-1计算):
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.2 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 | 10.6 |
(2)除钴的过程中,需要加入活化剂Sb2O3,锌粉会与Sb2O3等形成微电池产生合金CoSb.该微电池的正极反应式为Sb2O3+Co2++6H++10e-=2CoSb+3H2O
(3)除铁的过程分两步进行,①加入适量KMnO4,发生反应的离子方程式为3Fe2++MnO4-+4H+=3Fe3++MnO2+2H2O,②加入ZnO控制反应液的PH范围为3.3-7.2
(4)除铁过程第①步,若加入KMnO4时条件控制不当,MnO2会继续反应,造成的结果是,若加入的KMnO4不足量,则待电解溶液中有Fe元残余.请设计实验方案加以验证.
(5)净化后的溶液用惰性电极电解可获得镉单质.电解废液中可循环利用的溶质是H2SO4
(6)处理含镉废水常用化学沉淀法,以下是几种镉的难溶化合物的溶度积常数(25℃):
Kap(CdCO3)=5.2×10-12
Kap(CdS)=3.6×10-29
Kap(Cd(OH)2)=2.0×10-16,根据上述信息:
沉淀Cd2+效果最佳的试剂是b
a.Na2CO3 b.Na2S c.CaO
若采用生石灰处理含镉废水最佳PH为11,此时溶液中c(Cd2+)=2.0×10-10 mol•L-1.
5.X、Y、Z、M、W五种主族元素分属三个短周期,且原子序数依次增大.X、Z同族,可形成离子化合物ZX;Y′、M同主族,可形成MY2、MY3两种分子.下列说法中正确的是( )
| A. | 原子半径的大小:W>Z>X | |
| B. | 气态氢化物的还原性:Y>M | |
| C. | 最高价氧化物的水化物的酸性:M>W | |
| D. | X与Y可形成10电子分子和18电子分子 |
2.短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,Y原子最外层电子数是其内层电子总数的3倍,W原子的核电荷数等于X、Z原子的核电荷数之和,X和Z同主族.下列说法正确的是( )
| A. | 原子半径:r(W)>r(Z)>r(Y) | |
| B. | Z的最高价氧化物对应水化物的碱性比W的强 | |
| C. | 化合物X2Y2和Z2Y2所含化学键类型完全相同 | |
| D. | 工业上常用电解熔融W的氧化物制备W的单质 |
9.下列说法正确的是( )
| A. | 工业电解精炼铜时,粗铜与外电源的正极相连 | |
| B. | 常温下向纯水中加入盐酸,水的离子积减小 | |
| C. | 催化剂既能改变化学反应速率,也能改变焓变 | |
| D. | 其它条件不变时,升髙温度,吸热反应的v(正)增大,v(逆)减小 |
12.在电解水制取H2和O2时,为了增强导电性,常常在水中加入一些电解质,下列物质可选用( )
| A. | NaCl | B. | CuCl2 | C. | NaOH | D. | CuSO4 |