题目内容
14.下列关于常见物质的工业制法的叙述,不正确的是( )| A. | 工业制硅:用焦炭在高温下还原二氧化硅可制得高纯硅 | |
| B. | 工业冶炼铁:需要用到的原料有铁矿石、焦炭、空气和石灰石 | |
| C. | 工业冶炼镁:电解熔融的无水氯化镁,可以得到金属镁 | |
| D. | 工业制玻璃:将石灰石、纯碱、石英在玻璃熔炉中高温熔融制得 |
分析 A.焦炭在高温下还原二氧化硅得到粗硅;
B.工业炼铁原料中应有石灰石不是生石灰,工业炼铁高炉中发生的主要反应有:在高温下,焦炭跟氧气反应生成二氧化碳;二氧化碳被焦炭还原成一氧化碳;一氧化碳再跟铁矿石中的氧化物反应,生成铁,石灰石作用是除渣;
C.镁为活泼金属,可用电解法冶炼;
D.玻璃的主要成分为硅酸盐和二氧化硅.
解答 解:A.焦炭在高温下还原二氧化硅得到的 硅含有碳、碳化硅等杂质,为粗硅,为进一步提纯,可与氯气反应,再用氢气还原,故A错误;
B.业炼铁:需要用到的原料有铁矿石、焦炭、空气和石灰石,焦炭的作用:提供热量、生成一氧化碳;一氧化碳再跟铁矿石中的氧化物反应,生成铁,石灰石在高温条件下分解能生成氧化钙和二氧化碳,氧化钙能和铁矿石中的杂质二氧化硅反应生成硅酸钙,从而除去二氧化硅,故B正确;
C.镁为活泼金属,且熔融的氯化镁可导电,工业用电解法熔融的氯化镁的方法冶炼镁,故C正确;
D.玻璃的主要成分为硅酸盐和二氧化硅,可用石灰石、纯碱、石英为原料,故D正确.
故选A.
点评 本题考查常见物质的工业制法,涉及物质的性质与应用,为高考常见题型,侧重考查化学与生活、生产等知识,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
4.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )
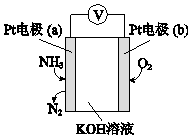

| A. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| B. | 电极a的反应式为2NH3-6e-+6OH-═N2+6H2O | |
| C. | O2在电极b上发生还原反应 | |
| D. | 溶液中OH-向电极a移动 |
5.下列说法正确的是( )
| A. | HCOOCH3和CH3CHO表示同一种物质 | |
| B. | C2H5OH在NaOH水溶液中加热,可发生消去反应生成乙烯 | |
| C. | 医用酒精的浓度通常为95% | |
| D. | 蛋白质遇到浓硝酸,得到黄色沉淀 |
2.氯化亚铜(CuCl,白色、易氧化,Ksp=1.2×10-6)广泛用作催化剂、脱臭剂、脱色剂等.工业上用初级铜矿粉(主要含Cu2S、CuS、Fe2O3、FeO等)制备活性CuCl的流程如图:
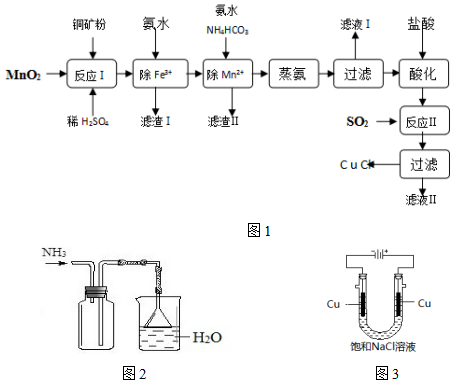
(1)滤渣Ⅰ是Fe(OH)3和单质硫的混合物,反应Ⅰ中Cu2S参与反应的化学方程式为:Cu2S+MnO2+H2SO4→CuSO4+S+MnSO4+H2O(未配平)
氧化产物为:CuSO4、S
(2)除Mn2+时得MnCO3沉淀,该反应的离子方程式Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O
(3)已知:Cu(OH)2可溶于氨水形成深蓝色溶液.Cu(OH)2+4NH3?[Cu(NH3)4]2++2OH-
蒸氨条件及蒸氨效果见表
由表中信息可知蒸氨的条件应选c(填序号).蒸出的氨可以回收利用,在实验室用图2装置来收集当集气瓶收集满氨时观察到的现象是漏斗中的液面忽上忽下.
(4)反应Ⅱ的离子方程式SO2+2Cu2++2Cl-+2H2O=2CuCl↓+SO42-+4H+.
(5)实验证明通过图3装置也可获得CuCl,现象为
阴极:产生无色气体
阳极:有白色胶状沉淀生成且逐渐增多
U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色沉淀,
①生成CuCl的电极反应式为Cu-e-+Cl-=CuCl↓.
②有同学提出说:淡黄色沉淀可能是CuOH,以下是从资料中查阅到的有关CuOH信息,哪些可以支持该同学的说法bd.(填序号)
a.容易脱水变成红色的Cu2O.
b.CuOH是黄色或淡黄色固体,不溶于水
c.价格:240元/Kg
d.CuOH的Ksp=2×10-15
e.易被氧化成Cu(OH)2.

(1)滤渣Ⅰ是Fe(OH)3和单质硫的混合物,反应Ⅰ中Cu2S参与反应的化学方程式为:Cu2S+MnO2+H2SO4→CuSO4+S+MnSO4+H2O(未配平)
氧化产物为:CuSO4、S
(2)除Mn2+时得MnCO3沉淀,该反应的离子方程式Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O
(3)已知:Cu(OH)2可溶于氨水形成深蓝色溶液.Cu(OH)2+4NH3?[Cu(NH3)4]2++2OH-
蒸氨条件及蒸氨效果见表
| 序号 | 温度/℃ | 时间/min | 压强/KPa | 残液颜色 |
| a | 110 | 60 | 101.3 | 浅蓝色 |
| b | 100 | 40 | 74.6 | 几乎很浅 |
| c | 90 | 30 | 60.0 | 无色透明 |
(4)反应Ⅱ的离子方程式SO2+2Cu2++2Cl-+2H2O=2CuCl↓+SO42-+4H+.
(5)实验证明通过图3装置也可获得CuCl,现象为
阴极:产生无色气体
阳极:有白色胶状沉淀生成且逐渐增多
U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色沉淀,
①生成CuCl的电极反应式为Cu-e-+Cl-=CuCl↓.
②有同学提出说:淡黄色沉淀可能是CuOH,以下是从资料中查阅到的有关CuOH信息,哪些可以支持该同学的说法bd.(填序号)
a.容易脱水变成红色的Cu2O.
b.CuOH是黄色或淡黄色固体,不溶于水
c.价格:240元/Kg
d.CuOH的Ksp=2×10-15
e.易被氧化成Cu(OH)2.
9.人们对原子结构的认识有一个不断深入的过程,其中提出“葡萄干面包”原子模型的科学家是( )
| A. | 道尔顿 | B. | 汤姆生 | C. | 卢瑟福 | D. | 玻尔 |
19.实验室保存下列化学试剂的方法不正确的是( )
| A. | 新制氯水放在棕色试剂瓶中,避光保存 | |
| B. | 液溴密封盛放在棕色瓶中,液面上放一层水 | |
| C. | 少量金属钠保存在四氯化碳中 | |
| D. | 水玻璃保存在带胶塞的玻璃试剂瓶中 |
6.m g铜与足量浓H2SO4共热时完全反应,收集到n L SO2,则被还原的H2SO4的物质的量是( )
| A. | $\frac{m}{32}$mol | B. | $\frac{m}{64}$mol | C. | $\frac{n}{11.2}$mol | D. | $\frac{n}{22.4}$mol |
7.运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为5KClO3+6P=3P2O5+5KCl.下列有关该反应的叙述不正确的是( )
| A. | KClO3是氧化剂 | B. | P2O5是氧化产物 | ||
| C. | 1molKClO3参加反应有6mole-转移 | D. | 每有6molP被还原,生成5molKCl |
 .
.