��Ŀ����
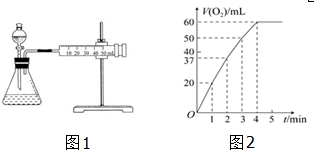
20��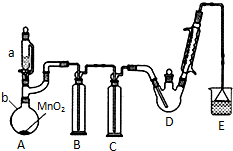 ij̽��С���������ͼ��ʾװ�ã��г֡����������ԣ���ģ�ҵ���������Ʊ�������ȩ��CCl3CHO����ʵ�飮 �������ϣ��й���Ϣ��ͼ��
ij̽��С���������ͼ��ʾװ�ã��г֡����������ԣ���ģ�ҵ���������Ʊ�������ȩ��CCl3CHO����ʵ�飮 �������ϣ��й���Ϣ��ͼ�����Ʊ���Ӧԭ����C2H5OH+4Cl2��CCl3CHO+5HCl
���ܷ����ĸ���Ӧ��C2H5OH+HCl��C2H5Cl+H2O
CCl3CHO+HClO��CCl3COOH+HCl
���������ᣩ
��������ʵIJ����������ʣ�
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| �۵�/�� | -114.1 | -57.5 | 58 | -138.7 |
| �е�/�� | 78.3 | 97.8 | 198 | 12.3 |
| �ܽ��� | ��ˮ���� | ������ˮ���Ҵ� | ������ˮ���Ҵ� | ����ˮ���������Ҵ� |
��2��װ��C������Ϊ��ȥ�����л��е�H2O������������������ɣ�װ��D�ɲ���ˮԡ���ȵķ����Կ��Ʒ�Ӧ�¶���70�����ң�
��3����Ӧ�������ܲ�ȡ�Ƚ�D�еĻ������ȴ�����£����ù��˵ķ��������CCl3COOH��ԭ��ΪCCl3COOH�����Ҵ���CCl3CHO��
��4��װ��E����ҺΪNaOH��Һ�����ܷ���������Ӧ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O��H++OH-=H2O��
��5���ⶨ��Ʒ���ȣ���ȡ��Ʒ0.30g��ɴ�����Һ������0.1000mol•L-1�����Һ20.00mL���ټ�������Na2CO3��Һ����Ӧ��ȫ�����������Һ��pH��������0.02000mol•L-1��Na2S2O3��Һ�ζ����յ㣮����ƽ��ʵ��������Na2S2O3��Һ20.00mL�����Ʒ�Ĵ���Ϊ88.5%����CCl3CHO����Է�������Ϊ147.5��
�ζ��ķ�Ӧԭ�����£�CCl3CHO+OH-=CHCl3+HCOO-HCOO-+I2=H++2I-+CO2��
I2+2S2O32-=2I-+S4O62-
��6����֪��������Ka��CCl3COOH��=1.0��10-1�� mol•L-1��Ka ��CH3COOH��=1.7��10-5�� mol•L-1
�����ʵ��֤���������ᡢ���������ǿ����
�ֱ�ⶨ0.1 mol•L-1��������Һ��pH�����������pH��С��֤���������������ǿ�����ᣮ
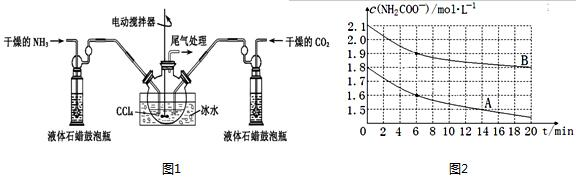
���� Aװ�����ö���������Ũ�����Ʊ�������Bװ���ñ���ʳ��ˮ��ȥHCl��Cװ��ʢ��Ũ�������������D�з�Ӧ�Ʊ�CCl4CHO��Eװ��ʢ������������Һ������β����������HCl��ֹ��Ⱦ������
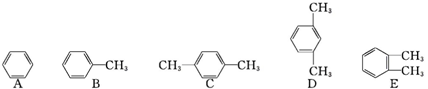
��1���������Ľṹ����֪bΪԲ����ƿ���ñ���ʳ��ˮ��ȥHCl������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ��
��2����ȥˮ����������������������ɣ����Ʒ�Ӧ�¶���70�����ң�Ӧ��ȡˮԡ���ȣ�
��3��CCl3COOH�����Ҵ���CCl3CHO��
��4��E��Ϊ����������Һ������������HCl��
��5���������ĵ�Na2S2O3����ʣ��I2�����ʵ���������������HCOO-��Ӧ��I2�����ʵ������ٸ��ݹ�ϵʽ��CCl3CHO��HCOO-��I2���㣻
��6���ɵ���ƽ�ⳣ����֪��������������Ա����������ǿ�����Բⶨ��ͬŨ�ȵ�pH��֤��
��� �⣺Aװ�����ö���������Ũ�����Ʊ�������Bװ���ñ���ʳ��ˮ��ȥHCl��Cװ��ʢ��Ũ�������������D�з�Ӧ�Ʊ�CCl4CHO��Eװ��ʢ������������Һ������β����������HCl��ֹ��Ⱦ������
��1���������Ľṹ����֪bΪԲ����ƿ��Bװ���ñ���ʳ��ˮ��ȥHCl�����ٸ���Ӧ��������ȥBװ�ã������л���HCl������ӦC2H5OH+HCl��C2H5Cl+H2O�ķ���������װ��D�и�����C2H5Cl���ࣻ
����������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ����Ӧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
�ʴ�Ϊ��Բ����ƿ������ʳ��ˮ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��Cװ��ʢ��Ũ���������������ȥˮ����������������������ɣ����Ʒ�Ӧ�¶���70�����ң�Ӧ��ȡˮԡ����
�ʴ�Ϊ����ȥ�����л��е�H2O������������������ɣ�ˮԡ��
��3��CCl3COOH�����Ҵ���CCl3CHO���ù��˵ķ��������CCl3COOH��Ӧ��ȡ�������з��룬
�ʴ�Ϊ��CCl3COOH�����Ҵ���CCl3CHO��
��4��Eװ��ʢ������������Һ������β����������HCl��ֹ��Ⱦ��������Ӧ���ӷ���ʽΪ��Cl2+2OH-=Cl-+ClO-+H2O��H++OH-=H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��H++OH-=H2O��
��5��ʣ��I2�����ʵ���0.02000mol•L-1��0.02L=2��10-4mol����HCOO-��Ӧ��I2�����ʵ���Ϊ0.1000mol•L-1��0.02L-2��10-4mol=1.8��10-3mol����CCl3CHO��HCOO-��I2��֪��CCl3CHO�����ʵ���Ϊ1.8��10-3mol�����Ʒ�Ĵ���Ϊ$\frac{1.8��1{0}^{-3}mol��147.5g/mol}{0.3g}$��100%=88.5%��
�ʴ�Ϊ��88.5%��
��6���ɵ���ƽ�ⳣ����֪��������������Ա����������ǿ��֤���������ᡢ���������ǿ����ʵ�鷽��Ϊ���ֱ�ⶨ0.1 mol•L-1��������Һ��pH�����������pH��С��֤���������������ǿ�����ᣬ
�ʴ�Ϊ���ֱ�ⶨ0.1 mol•L-1��������Һ��pH�����������pH��С��֤���������������ǿ�����ᣮ
���� ���⿼���л����Ʊ������ʺ����ⶨ��ʵ�鷽����ơ����ʵķ����ᴿ����װ�õķ������۵ȣ��ؼ�����ȷ��Ӧԭ�����װ�����ã����ճ������ʷ����ᴿ������ע�����Ŀ��Ϣ��Ӧ�ã��Ѷ��еȣ�

| A�� | NaOH  | B�� | H2S�� 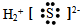 | C�� | N2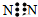 | D�� | CO2  |
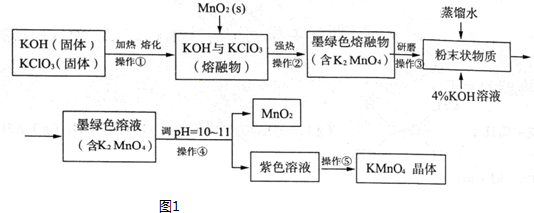
| t/min | 0 | 2 | 4 | 6 | 8 |
| V��O2��/mL | 0 | 9.9 | 17.2 | 22.4 | 26.5 |
��1��6min�ڹ�������ķֽ����ʣ�����ȷ��0.01��
��2��6min�ڹ�������ֽ��ת���ʣ�
��3��6min�ڹ�����������ʵ���Ũ�ȣ�
| A�� | 1��1 | B�� | 2��1 | C�� | 3��1 | D�� | 4��1 |