��Ŀ����
3�����ΪԪ�����ڱ���һ���ְ�Ҫ����ɸ�С�⣮| ���� �� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | O |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
| 4 | �� | �� |
��2���٢ۢ�����Ԫ�ص�����������ˮ�����У�������ǿ����NaOH
��3��Ԫ�آݵ����������Ϊ��������������ԡ����Ի��������������������������������Ʒ�Ӧ�Ļ�ѧ����ʽΪAl2O3+2NaOH=2NaAlO2+H2O�����Ԫ�غ͢��Ԫ����ɵĻ�������Һ�У������μ�����������Һ������������Ϊ�����ɰ�ɫ������������ܽ⣮
���� ��Ԫ�������ڱ���λ�ã���֪��ΪNa����ΪK����ΪMg����ΪCa����ΪAl����ΪC����ΪO����ΪF����ΪCl����ΪAr��
��1��ϡ������������ȶ���F�ķǽ�������ǿ��K�Ľ�������ǿ��K��ˮ��Ӧ����KOH��������
��2��ͬ���ڴ������ҽ����Լ�����������Խǿ����Ӧ����������ˮ�������Խǿ��
��3��Ԫ�آݵ����������Ϊ����������NaOH��Ӧ����ƫ�����ƺ�ˮ�������ᷴӦ�����Ȼ�����ˮ���ݺ͢��Ԫ����ɵĻ������Ȼ�������NaOH��Ӧ�����ɳ�����������ܽ⣮
��� �⣺��Ԫ�������ڱ���λ�ã���֪��ΪNa����ΪK����ΪMg����ΪCa����ΪAl����ΪC����ΪO����ΪF����ΪCl����ΪAr��
��1����ѧ��������õ�Ԫ��ΪAr���ǽ�������ǿ��Ԫ����F����������ǿ�ĵ�����ˮ��Ӧ�Ļ�ѧ����ʽΪ2K+2H2O=2KOH+H2����
�ʴ�Ϊ��Ar��F��2K+2H2O=2KOH+H2����
��2��ͬ���ڴ������ҽ����Լ�����������Խǿ����Ӧ����������ˮ�������Խǿ����٢ۢ�����Ԫ�ص�����������ˮ�����У�������ǿ����NaOH��
�ʴ�Ϊ��NaOH��
��3��Ԫ�آݵ����������Ϊ����������NaOH��Ӧ����ƫ�����ƺ�ˮ�������ᷴӦ�����Ȼ�����ˮ����Ԫ�آݵ����������Ϊ�����������������������������Ʒ�Ӧ�Ļ�ѧ����ʽΪAl2O3+2NaOH=2NaAlO2+H2O�����Ԫ�غ͢��Ԫ����ɵĻ�������Һ�У������μ�����������Һ������������AlCl3+3NaOH=Al��OH��3��+3NaCl��Al��OH��3+NaOH=NaAlO2+2H2O������Ϊ�����ɰ�ɫ������������ܽ⣬
�ʴ�Ϊ�����������Al2O3+2NaOH=2NaAlO2+H2O�������ɰ�ɫ������������ܽ⣮
���� ���⿼��λ�á��ṹ�����ʣ�Ϊ��Ƶ���㣬����Ԫ�ص�λ�á����ʡ�Ԫ�ػ�����֪ʶΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�����������������������ԣ���Ŀ�ѶȲ���

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | ��2 min�ڵķ�Ӧ������B��ʾΪ0.3 mol/��L•min�� | |
| B�� | ��2 min����A��ʾ��Ӧ������0.4 mol/��L•min�� | |
| C�� | ��2 min����C��ʾ��Ӧ������0.2 mol/��L•min�� | |
| D�� | ��V����B��=3V����D��ʱ����Ӧ�ﵽƽ�� |
| A�� | ��״���£�22.4L�����������Ļ�����壬����������ΪNA | |
| B�� | ���³�ѹ�£�1mol�������е�ԭ����Ϊ2NA | |
| C�� | 1molAl3+���к��������Ϊ10NA | |
| D�� | 17gNH3���еĵ�����Ϊ10NA |
 �о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����壮
�о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����壮��1��CO��������������֪��
Fe2O3��s��+3C��s��=2Fe��s��+3CO��g����H1=+489.0kJ•mol-1
C��s��+CO2��g��=2CO��g����H2=+172.5kJ•mol-1
��CO��ԭFe2O3��s�����Ȼ�ѧ����ʽΪFe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-28.5 kJ•mol-1��
��2�������¯ú���õ���CO���������Ƴ�ȼ�ϵ�أ��������Ϊ���ԣ�д����ȼ�ϵ�صĸ�����ӦʽCO+4OH--2e-=CO32-+2H2O��
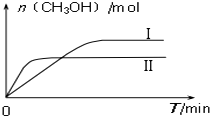
��3��CO2��H2����һ��������ܱ������У��������¶��·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g�������CH3OH�����ʵ�����ʱ��ı仯ͼ��
����ͼ�жϸ÷�Ӧ��H�� 0������ I��II��Ӧ��ƽ�ⳣ��KI��KII���������=����������
��һ���¶��£����ݻ���ͬ�ҹ̶��������ܱ������У������·�ʽ���뷴Ӧ�һ��ʱ���ﵽƽ�⣮
| �� �� | �� | �� |
| ��Ӧ��Ͷ���� | 1molCO2��3molH2 | a molCO2��b molH2�� c molCH3OH��g����c molH2O��g�� |
��һ���¶��£��˷�Ӧ�ں����ܱ������н��У����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������a b��
a��������ѹǿ���� b��H2������������� c��c��H2��=3c��CH3OH��
d���������ܶȲ��� e��2��C=O���ѵ�ͬʱ��3��C-H�γ�
��4����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��2CO2��g��+6H2��g��=CH3OCH3��g��+3H2O��g���������ѿ�����ֱ��ȼ�ϵ�أ�1mol�����ѷ��Ӿ����绯ѧ���������Բ���12NA�����ӵĵ��������ݻ�ѧ��Ӧԭ������������ѹǿ���Ʊ������ѷ�Ӧ��Ӱ��÷�Ӧ���������٣�ѹǿ����ʹƽ�����ƣ�CH3OCH3�������ӣ�ѹǿ����ʹCO��H2Ũ�����ӣ���Ӧ��������
| �� | �� | �� | �� | |
| �� | �� | �� |
��2����ѧ��ͨ���Ԣ١���Ԫ�صĻ���������о����Ӷ�Ѱ��a��ѡ����ţ���
a����Чũҩ b������
c�����¡���ʴ�ĺϽ���� d���뵼�����
��3���о��١���Ԫ�ص���̬�⻯��û�ѧ���Żش𣩣��ڵ���̬�⻯��ĵ���ʽ
 ��
����4���ܺ͢ݵ�Ԫ������������Ӧˮ��������Խ�ǿ�����ʵĻ�ѧʽH2SO4��
| A�� | ��n���ڵ����һ�ֽ���Ԫ�ش��ڵ�n���壨n��1�� | |
| B�� | m=1��m=7��Ԫ�ص��������ʱ�������γ����ӻ����� | |
| C�� | ��n������8-n�ַǽ���Ԫ�أ�n��1������ϡ������Ԫ�أ� | |
| D�� | m-n=5������Ԫ�ش��ڱ�������ǿ�Ķ�Ӧ������ |
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | ||
| 4 | �� | �� |
��2����������õĽ�����K���ǽ�����ǿ��Ԫ����F������дԪ�ط��ţ�
��3���������γ��������������Ԫ����Al���ֱ�д����Ԫ�ص�����������ޡ�������������ˮ���ﷴӦ�Ļ�ѧ����ʽ��2Al��OH��3+3H2SO4=Al2��SO4��3+6H2O��Al��OH��3+KOH=KAlO2+2H2O��
��4�������һ��ʵ�鷽�����ȽϢߡ��ⵥ�������Ե�ǿ�����û�ѧ����ʽ�����Cl2+2NaBr=Br2+2NaCl��
| A�� | Fe2++Cl2��Fe3++2Cl- | |
| B�� | 2Fe2++2Br-+2I-+3Cl2=2Fe3++I2+Br2+6Cl- | |
| C�� | 2Fe2++4Br-+2I-+4Cl2��2Fe3++I2+2Br2+8Cl- | |
| D�� | 4Fe2++2Br-+2I-+4Cl2=4Fe3++I2+Br2+8Cl- |