题目内容
8.根据以下叙述和元素周期表的有关知识,回答下题:主族元素的性质主要由其原子的最外层电子数和电子层数决定,若元素的最外层电子数为m,电子层数为n,一般具有这样的规律:m>n的元素为非金属元素,m≤n的元素为金属元素.下列有关推断符合实际的是( )| A. | 第n周期的最后一种金属元素处在第n主族(n>1) | |
| B. | m=1与m=7的元素单质相互化合时,都能形成离子化合物 | |
| C. | 第n周期有8-n种非金属元素(n>1,包括稀有气体元素) | |
| D. | m-n=5的主族元素存在本周期最强的对应含氧酸 |
分析 A.金属元素的最外层电子数≤周期数,第n周期的最后一种金属元素最外层电子数为n,为主族元素,族序数等于最外层电子数;
B.H和Cl形成的化合物为HCl,是共价化合物;
C.第2周期有2种主族金属元素为Li、Be,第3周期有3种主族金属元素为Na、Mg、Al,类推判断;
D.最强的含氧酸为HClO4,其中Cl元素最外层电子数-电子层数=4.
解答 解:A.金属元素的最外层电子数≤周期数,第n周期的最后一种金属元素最外层电子数为n,为主族元素,族序数等于最外层电子数,该处于第n主族,故A正确;
B.H和Cl形成的化合物为HCl,是共价化合物,故B错误;
C.第2周期有2种主族金属元素为Li、Be,第3周期有3种主族金属元素为Na、Mg、Al,类推知第n周期有n种主族金属元素,故C正确;
D.m-n=5的主族元素对应含氧酸的酸性不一定最强,如第三周期中酸性最强的含氧酸为HClO4,而Cl元素最外层电子数-电子层数=4,故D错误;
故选AC.
点评 本题考查元素周期表的结构和应用,题目难度不大,注意把握元素周期表的结构特点,学习中善于把握相关组成规律,在解答题目时会起到事半功倍的作用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.侯氏制碱法是将CO2通入含NH3的饱和NaCl溶液中,结晶,析出NaHCO3,过滤,将NaHCO3加热分解制得Na2CO3.母液加入NaCl,通入NH3,降温,结晶析出NH4Cl,使母液又成为含NH3的饱和NaCl溶液.下列说法错误的是( )
| A. | 侯氏制碱法的主要原料是NaCl、CO2和NH3 | |
| B. | Na2CO3的热稳定性低于NaHCO3 | |
| C. | 该方法的副产物是NH4Cl | |
| D. | 母液可循环利用 |
3.如表为元素周期表的一部分按要求完成各小题.
(1)化学性质最不活泼的元素Ar(填化学式,下同),非金属性最强的元素是F,金属性最强的单质与水反应的化学方程式为2K+2H2O=2KOH+H2↑
(2)①③⑤三种元素的最高价氧化物的水化物中,碱性最强的是NaOH
(3)元素⑤的最高价氧化物为两性氧化物(填酸性、碱性或两性氧化物),该最高价氧化物与氢氧化钠反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O;向该元素和⑨号元素组成的化合物溶液中,缓缓滴加氢氧化钠溶液至过量,现象为先生成白色沉淀,后沉淀溶解.
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)①③⑤三种元素的最高价氧化物的水化物中,碱性最强的是NaOH
(3)元素⑤的最高价氧化物为两性氧化物(填酸性、碱性或两性氧化物),该最高价氧化物与氢氧化钠反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O;向该元素和⑨号元素组成的化合物溶液中,缓缓滴加氢氧化钠溶液至过量,现象为先生成白色沉淀,后沉淀溶解.
13.如表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题.
(1)这10种元素中,形成化合物种类最多的元素是碳(写元素名称).
(2)元素①②③最高价氧化物对应的水化物中呈两性的物质的名称是氢氧化铝.
写出实验室制取该物质,反应的离子方程式为:Al3++3NH3.H2O=Al(OH)3+3NH4+.
(3)在检验某溶液是否含有①元素时,常用焰色反应.
(4)④和⑦形成化合物的化学键为:共价键.
(5)元素⑥.⑨最高价氧化物的化学式分别为:P2O5、Cl2O7.
| 族 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 2 | ④ | ⑦ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑥ | ⑧ | ⑨ | ⑩ |
(2)元素①②③最高价氧化物对应的水化物中呈两性的物质的名称是氢氧化铝.
写出实验室制取该物质,反应的离子方程式为:Al3++3NH3.H2O=Al(OH)3+3NH4+.
(3)在检验某溶液是否含有①元素时,常用焰色反应.
(4)④和⑦形成化合物的化学键为:共价键.
(5)元素⑥.⑨最高价氧化物的化学式分别为:P2O5、Cl2O7.
20.下列应用和相应原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应 | |
| B. | 我国古代的“湿法炼铜”:2Fe+3CuSO4=3Cu+Fe2(SO4)3置换反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 证明金属镁的活动性比铁强:3Mg+2Fe(OH)3=3Mg(OH)2+2Fe 置换反应 |
17.已知:SO32-+I2+H2O=SO42-+2I-+2H+.某溶液中可能含有Na+、NH4+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等.向该无色溶液中滴加少量溴水,溶液仍呈无色.下列关于该溶液的判断正确的是( )
| A. | 肯定不含I- | B. | 肯定含SO42- | C. | 肯定含有SO32- | D. | 肯定含有NH4+ |
18.NA为阿伏加德罗常数,下列描述正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 40 g NaOH溶解在1 L水中,所制得的溶液,物质的量浓度为1 mol•L-1 | |
| C. | 标准状况下,11.2 L四氯化碳所含分子数为0.5NA | |
| D. | 常温常压下,5.6g铁与过量的盐酸反应转移电子总数为0.2NA |
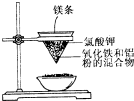 用如图所示的装置进行实验,回答下列问题:
用如图所示的装置进行实验,回答下列问题: