题目内容
10.下列说法不正确的是( )| A. | 食盐和醋都是常用的食品添加剂 | |
| B. | 钙、铁、碘都是人体内必需的微量元素 | |
| C. | ClO2、O3等均可用于饮用水消毒 | |
| D. | 静脉滴注NaHCO3溶液可治疗水杨酸中毒反应 |
分析 A.食盐有咸味,醋有酸味;
B.人体中的常量元素主要有:氧、碳、氢、氮、钙、磷、钾、硫、钠、氯、镁;微量元素主要有:铁、钴、铜、锌、铬、锰、钼、氟、碘、硒.铁、锌属于微量元素;
C.ClO2、O3等有强氧化性;
D.阿司匹林含有官能团有酯基和羧基,阿司匹林的溶液呈酸性.
解答 解:A.食盐有咸味,醋有酸味,可做食品添加剂,故A正确;
B.钙属于常量元素,故B错误;
C.ClO2、O3等有强氧化性,可用于饮用水消毒,故C正确;
D.长期服用阿司匹林会出现水杨酸中毒反应,应用碱性物质进行中和,碳酸氢钠具有碱性且碱性不强,所以可静脉注射碳酸氢钠溶液缓解,故D正确.
故选B.
点评 本题考查化学与生产、生活的关系,题目难度不大,要求学生能够用化学知识解释化学现象,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
20.H2CO3和H2C2O4都是二元弱酸,不同pH环境下它们不同形态的粒子的组成百分率如图所示,下列判断正确的是( )


| A. | 在pH为6.37及10.25时,溶液中c(CO32-)=c(HCO3-)=c(H2CO3) | |
| B. | 反应HCO3-+H2O═H2CO3+OH- 的平衡常数为10-10.25 | |
| C. | 0.1mol•L-1NaHC2O4溶液中c(HC2O4-)+c(C2O42-)+c(H2C2O4)=0.1mol•L-1 | |
| D. | 往Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4═HC2O4-+HCO3- |
1.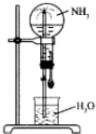 四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
 四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )| A. | ①>②>③>④ | B. | ①=②=③=④ | C. | ①=②=③>④ | D. | ①=②>③>④ |
2.辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2).一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
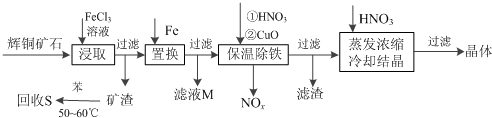
已知:部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表
(1)写出浸取过程中Cu2S溶解成Cu2+的离子方程式Cu2S+4Fe3+=2Cu2++4Fe2++S.
(2)气体NOx 与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为4NOx+(5-2x)O2+2H2O=4HNO3
(3)可向滤液M中加入(或通入)下列D(填字母)物质,得到较多的另一种可循环利用的物质.
A.Fe B.NaClO C.H2O2 D.Cl2
(4)蒸发浓缩时,要用硝酸调节溶液的pH,其作用是调节溶液pH使使铁元素完全转化为氢氧化铁沉淀,抑制铜离子水解.
(5)在除铁阶段,如果pH控制不当会使产量降低.你认为应该采取的补救措施是:将滤渣加入到HNO3中将pH调为3.7-4.7,充分反应后过滤,将滤液与原滤液合并.

已知:部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
(2)气体NOx 与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为4NOx+(5-2x)O2+2H2O=4HNO3
(3)可向滤液M中加入(或通入)下列D(填字母)物质,得到较多的另一种可循环利用的物质.
A.Fe B.NaClO C.H2O2 D.Cl2
(4)蒸发浓缩时,要用硝酸调节溶液的pH,其作用是调节溶液pH使使铁元素完全转化为氢氧化铁沉淀,抑制铜离子水解.
(5)在除铁阶段,如果pH控制不当会使产量降低.你认为应该采取的补救措施是:将滤渣加入到HNO3中将pH调为3.7-4.7,充分反应后过滤,将滤液与原滤液合并.
19.除去Na2CO3固体中少量NaHCO3的最好方法是( )
| A. | 加NaOH溶液 | B. | 加热 | C. | 加稀盐酸 | D. | 加Ca(OH)2溶液 |
20.第三周期元素R,它的原子最外电子层达到稳定结构所所需的电子数少于次外层与最内层电子数之差,且等于最内层电子数的整数倍,关于R的叙述中正确的是( )
| A. | 常温下,能稳定存在的R的氧化物都是酸性氧化物 | |
| B. | R的气态氢化物的水溶液具有强酸性 | |
| C. | R是金属元素 | |
| D. | R的气态氧化物不能在氧气中燃烧 |
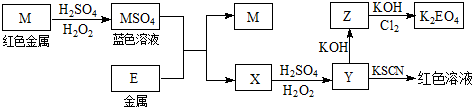


 (R、R′可以是氢原子、烃基或官能团)
(R、R′可以是氢原子、烃基或官能团) .
. .
. .
.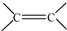 和
和 结构的D的所有同分异构共有7种(不包括顺反异构体),写出其中任意两种的结构简式CH2=CHCH2COOH、CH3CH=CHCOOH、CH2=CHCOOCH3、HCOOCH2CH=CH2、HCOOCH=CHCH3、CH3COOCH=CH2、HCOOC(CH3)=CH2(其中任两种).
结构的D的所有同分异构共有7种(不包括顺反异构体),写出其中任意两种的结构简式CH2=CHCH2COOH、CH3CH=CHCOOH、CH2=CHCOOCH3、HCOOCH2CH=CH2、HCOOCH=CHCH3、CH3COOCH=CH2、HCOOC(CH3)=CH2(其中任两种).