题目内容
1.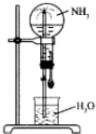 四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )
四个等体积的圆底烧瓶分别充满①NH3②HCl③NO2④NO2和O2的混合物进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量浓度大小关系为( )| A. | ①>②>③>④ | B. | ①=②=③=④ | C. | ①=②=③>④ | D. | ①=②>③>④ |
分析 相同条件下,等体积的气体其物质的量相等,氨气和氯化氢极易溶于水,则盛有等体积氯化氢、氨气的烧瓶分别倒立在水槽中时,水会充满整个烧瓶;二氧化氮和水反应方程式为:3NO2+H2O═2HNO3+NO,根据方程式可知,水充入烧瓶容积的$\frac{2}{3}$,如混有氧气,发生与二氧化氮进一步反应生成硝酸,根据c=$\frac{n}{V}$计算溶液的物质的量浓度.
解答 解:①设体积为3L,纯净的氨气,完全溶于水,溶液的体积等于烧瓶容积,所以溶液浓度为$\frac{3mol}{3mol×22.4L/mol}$=$\frac{1}{22.4}$mol/L;
②HCl完全溶于水,所以溶液物质的量浓度为$\frac{3mol}{3mol×22.4L/mol}$=$\frac{1}{22.4}$mol/L;
③纯净的NO2气体,发生反应3NO2+H2O=2HNO3+NO,生成硝酸2mol,1molNO,所以溶液体积等于烧瓶容积的$\frac{2}{3}$,所以溶液的物质的量浓度为$\frac{2mol}{2×22.4L}$=$\frac{1}{22.4}$mol/L;
④混有少量O2的NO2气体,把NO2分成两部分:第一部分:4NO2+O2+2H2O=4HNO3,由于O2很少,故还有:第二部分:3NO2+H2O=2HNO3+NO.这样第一部分反应中,5份的气体(4NO2+O2)生成4份HNO3,这部分溶液体积等于二氧化氮与氧气的体积,故这部分的浓度为$\frac{4mol}{5×22.4L}$=$\frac{1}{28}$mol/L,第二部分浓度为=$\frac{1}{22.4}$mol/L.所以比只有NO2气体形成的溶液浓度小.
故溶液浓度①=②=③>④.
故选:C.
点评 本题考查物质的量浓度计算,浓度中等,注意④中把整体分为两部分考虑.关键是判断溶液体积与气体的体积关系.

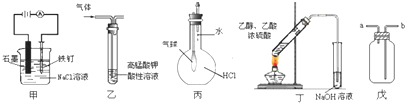
①装置甲可以防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可以验证HCl在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、HCl、NO2等气体.
| A. | ①⑤ | B. | ②③ | C. | ③⑤ | D. | ④⑤ |
| A. | 上述反应为化合反应 | |
| B. | “通路”是胶体对光产生的丁达尔现象 | |
| C. | 上述反应为氧化还原反应 | |
| D. | 产生的臭氧有毒,会严重影响人体健康 |
| A. | 反应中共消耗1.75 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为1:4 | ||
| C. | 反应中共消耗65 g Zn | D. | 反应中共转移3.6 mol电子 |
| A. | 托盘天平 | B. | 容量瓶 | C. | 玻璃棒 | D. | 胶头滴管 |
| A. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+28.7 kJ/mol | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-28.7 kJ/mol | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.4 kJ/mol | |
| D. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ/mol |
| A. | 食盐和醋都是常用的食品添加剂 | |
| B. | 钙、铁、碘都是人体内必需的微量元素 | |
| C. | ClO2、O3等均可用于饮用水消毒 | |
| D. | 静脉滴注NaHCO3溶液可治疗水杨酸中毒反应 |

 .
.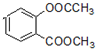 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+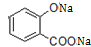 +H2O.
+H2O.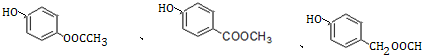 .
.