题目内容
13.在水中加入下列物质,能促进水的电离的是( )| A. | H2SO4 | B. | KOH | C. | FeCl3 | D. | Ba (NO3)2 |
分析 酸和碱能抑制水的电离,盐类的水解能促进水的电离,据此分析.
解答 解:A、硫酸电离出的氢离子能抑制水的电离,故A错误;
B、KOH电离出的氢氧根能抑制水的电离,故B错误;
C、氯化铁是强酸弱碱盐,在溶液中能结合水电离出的氢氧根而水解,故对水的电离有促进作用,故C正确;
D、硝酸钡是强酸强碱盐,在溶液中不水解,对水的电离无影响,故D错误.
故选C.
点评 本题考查了酸碱和能水解的盐对水的电离的影响,难度不大,应注意的是只有能水解的盐才对水的电离有促进.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
3.下列现象或事实能用同一原理解释的是( )
| A. | 常温下铁和铂都不溶于浓硫酸 | |
| B. | 硫化钠和硅酸钠固体长期基露在空气中变质 | |
| C. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| D. | SO2 和漂白液都能使品红溶液褪色 |
18.在甲酸溶液中加入一定量的NaOH溶液,恰好完全反应,对于生成的溶液,下列判断一定正确的是( )
| A. | c(HCOO-)<c(Na+) | B. | c(HCOO-)>c(Na+) | C. | c(OH-)>c(HCOO-) | D. | c(OH-)<c(HCOO-) |
5.除去苯中少量苯酚的方法是( )
| A. | 加FeCl3溶液、分液 | B. | 加浓溴水、过滤 | ||
| C. | 加液溴反应后蒸馏 | D. | 加NaOH溶液、分液 |
3.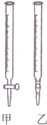 某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取25.0mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B.用标准NaOH溶液润洗滴定管2~3次
C.把盛有标注NaOH溶液的滴定管固定好,挤压玻璃球,使滴定管尖嘴充满溶液
D.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面值“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,进行滴定操作到终点,并记下滴定管液面的读数
回答下列问题:
(1)如图中属于酸式滴定管的甲(选填“甲”、“乙”).
(2)正确操作步骤的顺序是BDCEAF(填字母序号).
(3)上述B步操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)判断到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色.
(5)下列哪些操作会使测定结果偏高AC(填序号).
A.碱式滴定管用蒸馏水洗净后未用标准液润洗
B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)若平行实验三次,记录的数据如下表
试计算待测盐酸的物质的量浓度为0.0800mol•L-1.
 某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
某学生用0.1000mol•L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:A.移取25.0mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B.用标准NaOH溶液润洗滴定管2~3次
C.把盛有标注NaOH溶液的滴定管固定好,挤压玻璃球,使滴定管尖嘴充满溶液
D.取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面值“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,进行滴定操作到终点,并记下滴定管液面的读数
回答下列问题:
(1)如图中属于酸式滴定管的甲(选填“甲”、“乙”).
(2)正确操作步骤的顺序是BDCEAF(填字母序号).
(3)上述B步操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)判断到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色.
(5)下列哪些操作会使测定结果偏高AC(填序号).
A.碱式滴定管用蒸馏水洗净后未用标准液润洗
B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)若平行实验三次,记录的数据如下表
| 滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
| 滴定前读数(/mL) | 滴定后读数(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 0.00 | 22.99 |
| 3 | 25.00 | 0.20 | 20.19 |
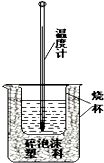 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题: