题目内容
5.除去苯中少量苯酚的方法是( )| A. | 加FeCl3溶液、分液 | B. | 加浓溴水、过滤 | ||
| C. | 加液溴反应后蒸馏 | D. | 加NaOH溶液、分液 |
分析 苯酚与NaOH反应后,与苯分层,然后分液可除杂,以此来解答.
解答 解:A.氯化铁可检验苯酚,不用于除杂,故A不选;
B.溴、三溴苯酚均易溶于苯,易引入新杂质,故B不选;
C.溴易溶于苯,不能除杂,故C不选;
D.苯酚与NaOH反应后,与苯分层,然后分液可除杂,故D选;
故选D.
点评 本题考查混合物分离提纯,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的性质、性质差异及混合物分离方法选择为解答该类题目的关键,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
15.下列关于硫酸的叙述正确的是( )
| A. | 浓硫酸具有吸水性 | B. | 稀硫酸可用铁罐贮存 | ||
| C. | 稀硫酸能使蔗糖脱水 | D. | SO2溶于水,可得到稀硫酸 |
16.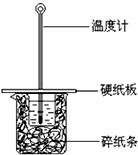 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )| A. | 采用0.55mol/L的NaOH溶液是保证盐酸完全被中和 | |
| B. | 图中实验装置缺少环形玻璃搅拌棒 | |
| C. | 烧杯间填满碎纸条的作用是保温隔热,防止热量损失 | |
| D. | 若烧杯上不盖硬纸板,测得的△H将偏小 |
13.在水中加入下列物质,能促进水的电离的是( )
| A. | H2SO4 | B. | KOH | C. | FeCl3 | D. | Ba (NO3)2 |
20.在0.1mol•L-1醋酸溶液中加入少量0.1mol•L-1盐酸,下列叙述正确的是( )
| A. | CH3COOH的电离程度增大,c(H+)增大 | |
| B. | 平衡向生成CH3COOH移动,c(H+)减小 | |
| C. | CH3COOH电离程度减小,pH减小 | |
| D. | 电离平衡向生成CH3COO-、H+方向移动,pH减小 |
10.如图是有关电化学的图示,完全正确的是( )
| A. | 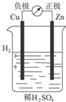 Cu-Zn原电池 | B. | 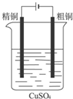 粗铜的精炼 | C. | 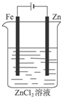 铁片镀锌 | D. | 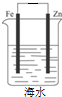 减缓铁腐蚀 |
17.下表列出A~K九种元素在周期表中的位置:
(1)请写出下列元素的元素符号ANaBKDAlGO..
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
(3)ABC这三种元素的原子半径由大到小的顺序排列为K>Na>Mg.(写出元素符号)
(4)G元素氢化物的化学式是H2O,该氢化物在常温下跟B反应的化学方程式为2K+2H2O=2KOH+H2↑,所得溶液的PH>7.(填>、=、<)
(5)在该周期表中,最高价氧化物对应的水化物中碱性最强的是KOH;最高价氧化物对应的水化物中酸性最强的是HClO4;气态氢化物最稳定的是HF.(写出物质的化学式)
| 周 期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VII A | 0 |
| 2 | E | G | H | |||||
| 3 | A | C | D | I | K | |||
| 4 | B | J |
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
(3)ABC这三种元素的原子半径由大到小的顺序排列为K>Na>Mg.(写出元素符号)
(4)G元素氢化物的化学式是H2O,该氢化物在常温下跟B反应的化学方程式为2K+2H2O=2KOH+H2↑,所得溶液的PH>7.(填>、=、<)
(5)在该周期表中,最高价氧化物对应的水化物中碱性最强的是KOH;最高价氧化物对应的水化物中酸性最强的是HClO4;气态氢化物最稳定的是HF.(写出物质的化学式)
14.下列关于NH4N03、KN03的说法正确的是( )
| A. | NH4N03是离子化合物,KN03是共价化合物 | |
| B. | NH4N03是共价化合物,KN03是离子化合物 | |
| C. | NH4N03和KN03都是离子化合物 | |
| D. | NH4N03和KN03都是共价化合物 |
15.25℃时下列叙述不正确的是( )
| A. | pH=3的二元弱酸H2R溶液与p=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液中:2c(R2-)+c(HR-)=(Na+) | |
| B. | 若0.3mol•L-1HY溶液与0.3mol•L-1NaOH溶液等体积混合后,溶液的pH=9,则:c(OH-)-c(HY)=(H+)=1×10-9mol•L-1 | |
| C. | 0.2mol•L-1HCl溶液与等体积0.05mol•L-1Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 0.1mol•L-1Na2S与0.1mol•L-1NaHS等体积混合:3c(Na+)-2c(HS-)=2c(S2-)+2c(H2S) |