题目内容
8.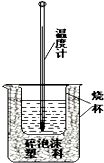 实验室利用如图装置进行中和热的测定.回答下列问题:
实验室利用如图装置进行中和热的测定.回答下列问题:(1)该图中有两处实验用品未画出,它们是环形玻璃搅拌棒、烧杯上方盖硬纸板;
(2)在操作正确的前提下提高中和热测定的准确性的关键是:提高装置的保温效果.
(3)请说明碎泡沫塑料的作用减少实验过程中的热量损失.
(4)如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将偏大 (填“偏大”、“偏小”、“不变”)原因是氢氧化钠固体溶于水放热.
分析 (1)根据量热计的构造来判断该装置的缺少仪器;根据中和热测定实验成败的关键是保温工作;
(2)根据在中和反应中,必须确保热量不散失;
(3)中和热测定实验成败的关键是保温工作;
(4)氢氧化钠固体溶于水放出热量.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,为了减少热量的损失,烧杯上方盖硬纸板;
故答案为:环形玻璃搅拌棒;烧杯上方盖硬纸板;
(2)在中和反应中,必须确保热量不散失;
故答案为:提高装置的保温效果;
(3)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失;
故答案为:减少实验过程中的热量损失;
(4)氢氧化钠固体溶于水放热,温度偏高,所以实验中测得的“中和热”数值将偏大;
故答案为:偏大;氢氧化钠固体溶于水放热.
点评 本题考查化学实验基本操作和中和热测定的实验,保温工作是实验成功的关键,难度不大.

练习册系列答案
相关题目
18.用氯气消毒过的自来水配制下列溶液时,会使所配溶液的溶质发生变化的是( )
①NaOH ②AgNO3 ③Na2CO3 ④NaBr ⑤FeCl2.
①NaOH ②AgNO3 ③Na2CO3 ④NaBr ⑤FeCl2.
| A. | 只有①② | B. | 只有①④⑤ | C. | 只有②④⑤ | D. | ①②③④⑤ |
19.下列物质中,可作为绿色燃料的是( )
| A. | 汽油 | B. | 煤 | C. | 石油 | D. | 氢气 |
16.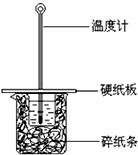 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
 某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )
某同学按照课本实验要求,用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法,不正确的是( )| A. | 采用0.55mol/L的NaOH溶液是保证盐酸完全被中和 | |
| B. | 图中实验装置缺少环形玻璃搅拌棒 | |
| C. | 烧杯间填满碎纸条的作用是保温隔热,防止热量损失 | |
| D. | 若烧杯上不盖硬纸板,测得的△H将偏小 |
3.某校化学实验小组探究浓度对化学反应速率的影响,并测定(NH4)2S2O8和KI反应的化学反应速率.进行如下实验探究:
【实验原理】
(NH4)2S2O8和KI反应的离子方程式为:S2O82-+2I-=2SO42-+I2
(1)实验时,向KI、Na2S2O3和淀粉指示剂混合溶液中加入(NH4)2S2O8溶液,不断搅拌.
在反应(1)进行的同时,发生反应:2S2O32-+I2=S4O62-+2I-
(2)反应(1)生成的I2立即与S2O32-反应,生成无色的S4O62-和I-.S2O32-耗尽时,反应(1)继续生成的I2才与淀粉作用呈现蓝色.从加入(NH4)2S2O8溶液到出现蓝色的时间为△t.
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上.
a=8.0 b=5 c=15
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是搅拌.
(3)第①组实验的v(S2O82-)=2.5×10-5mol•(L•s)-1.
(4)根据上表数据分析,可以得到的结论有(写出一条即可)S2O82-或I-的浓度越小,反应速率越慢.
【实验原理】
(NH4)2S2O8和KI反应的离子方程式为:S2O82-+2I-=2SO42-+I2
(1)实验时,向KI、Na2S2O3和淀粉指示剂混合溶液中加入(NH4)2S2O8溶液,不断搅拌.
在反应(1)进行的同时,发生反应:2S2O32-+I2=S4O62-+2I-
(2)反应(1)生成的I2立即与S2O32-反应,生成无色的S4O62-和I-.S2O32-耗尽时,反应(1)继续生成的I2才与淀粉作用呈现蓝色.从加入(NH4)2S2O8溶液到出现蓝色的时间为△t.
【实验内容】
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上.
| 实 验 编 号 | ① | ② | ③ | ④ | ⑤ | |
试剂 用量 (mL) | 0.20mol•L-1(NH4)2 S2O8溶液 | 20.0 | 10.0 | b | 20.0 | 20.0 |
| 0.20mol•L-1KI溶液 | 20.0 | 20.0 | 20.0 | 10.0 | 5.0 | |
| 0.010mol•L-1 Na2S2O3溶液 | a | 8.0 | 8.0 | 8.0 | 8.0 | |
| 0.2% 淀粉溶液 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 0.20mol•L-1KNO3溶液 | 0 | 0 | 0 | 10.0 | c | |
| 0.20mol•L-1(NH4)2SO4溶液 | 0 | 10.0 | 15.0 | 0 | 0 | |
| 20℃时,反应时间△t(s) | 32 | 67 | 130 | 66 | 135 | |
| 为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 | ||||||
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是搅拌.
(3)第①组实验的v(S2O82-)=2.5×10-5mol•(L•s)-1.
(4)根据上表数据分析,可以得到的结论有(写出一条即可)S2O82-或I-的浓度越小,反应速率越慢.
13.在水中加入下列物质,能促进水的电离的是( )
| A. | H2SO4 | B. | KOH | C. | FeCl3 | D. | Ba (NO3)2 |
20.在0.1mol•L-1醋酸溶液中加入少量0.1mol•L-1盐酸,下列叙述正确的是( )
| A. | CH3COOH的电离程度增大,c(H+)增大 | |
| B. | 平衡向生成CH3COOH移动,c(H+)减小 | |
| C. | CH3COOH电离程度减小,pH减小 | |
| D. | 电离平衡向生成CH3COO-、H+方向移动,pH减小 |
17.下表列出A~K九种元素在周期表中的位置:
(1)请写出下列元素的元素符号ANaBKDAlGO..
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
(3)ABC这三种元素的原子半径由大到小的顺序排列为K>Na>Mg.(写出元素符号)
(4)G元素氢化物的化学式是H2O,该氢化物在常温下跟B反应的化学方程式为2K+2H2O=2KOH+H2↑,所得溶液的PH>7.(填>、=、<)
(5)在该周期表中,最高价氧化物对应的水化物中碱性最强的是KOH;最高价氧化物对应的水化物中酸性最强的是HClO4;气态氢化物最稳定的是HF.(写出物质的化学式)
| 周 期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VII A | 0 |
| 2 | E | G | H | |||||
| 3 | A | C | D | I | K | |||
| 4 | B | J |
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
(3)ABC这三种元素的原子半径由大到小的顺序排列为K>Na>Mg.(写出元素符号)
(4)G元素氢化物的化学式是H2O,该氢化物在常温下跟B反应的化学方程式为2K+2H2O=2KOH+H2↑,所得溶液的PH>7.(填>、=、<)
(5)在该周期表中,最高价氧化物对应的水化物中碱性最强的是KOH;最高价氧化物对应的水化物中酸性最强的是HClO4;气态氢化物最稳定的是HF.(写出物质的化学式)
18.鉴别乙醇和汽油,最简单的方法是( )
| A. | 加金属钠,有气体产生的是乙醇 | |
| B. | 加水,互溶的是乙醇 | |
| C. | 点燃,容易燃烧的是乙醇 | |
| D. | 和浓硫酸混合共热至170℃,有乙烯产生的是乙醇 |