题目内容
10. 锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”.
锂离子电池广泛应用于日常电子产品中,也是电动汽车动力电池的首选.正极材料的选择决定了锂离子电池的性能.磷酸铁钾(LiFePO4)以其高倍率性、高比能量、高循环特性、高安全性、低成本、环保等优点而逐渐成为“能源新星”.(1)磷酸铁锂电池比钻酸锂电池或锰酸锂电池更环保的原因是磷酸铁锂电池不会产生重金属污染.
(2)高温固相法是磷酸铁锂生产的主要方法.通常以铁盐、磷酸盐和锂盐为原料,按化学计量比充分混匀后,在惰性气氛的保护中先经过较低温预分解,再经高温焙烧,研磨粉碎制成.
其反应原理如下:①完成上述化学方程式.
Li2CO3+2FeC2O4•2H2O+2NH4H2PO4═2LiFePO4+2NH3↑+3CO2↑+2CO↑+7H2O↑
②理论上,反应中每转移0.15mol电子,会生成LiFePO423.7g.
③反应需在惰性气氛的保护中进行,其原因是防止Fe(II)被氧化.
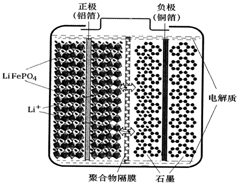
(3)磷酸铁锂电池装置如图所示,其中正极材料橄榄石型LiFePO4通过粘合剂附着在铝箔表面,负极石墨材料附着在铜箔表面,电解质为溶解在有机溶剂中的锂盐.
电池工作时的总反应为:LiFePO4+6C$?_{放电}^{充电}$Li1-xFePO4+LixC6,则放电时,正极的电极反应式为Li1-xFePO4+xLi++xe-═LiFePO4.充电时,Li+迁移方向为由左向右(填“由左向右”或“由右向左”),图中聚合物隔膜应为阳(填“阳”或“阴”)离子交换膜.
(4)废旧磷酸铁锂电池的正极材料(主要成分为LiFePO4,难溶于水,不与强碱反应)可通过湿法回收锂和铁,其过程如下:
①碱溶.加入强碱溶液除去铝箔及其氧化物,过滤.
②酸浸.在过滤后的滤渣中加入H2SO4和H2O2的混合溶液,发生反应的离子方程式为2LiFePO4+2H++H2O2═2Li++2Fe3++2PO43-+2H2O,得到浸出液.
③分离锂和铁.向浸出液中加碱调节溶液的pH使铁元素沉淀,当pH为2.7时,铁恰好沉淀完全(已知Ksp[Fe(OH)3]=1×10-39当离子浓度小于l×10-5mo1•L-1时,可认为该离子沉淀完全)
分析 (1)重金属离子会产生污染;
(2)①根据原子守恒分析;
②C2O42-中C的化合价为+3价,生成CO和CO2,C元素的化合价分别为+2价、+3价,根据电子与LiFePO4的关系计算;
③亚铁离子容易被氧气氧化;
(3)放电时,Li1-xFePO4在正极上得电子发生还原反应;充电时,阳离子向阴极移动;电解质为锂盐,锂离子通过交换膜向正极移动;
(4)②LiFePO4中亚铁离子在酸性条件下,被双氧水氧化为铁离子;
③当离子浓度小于l×10-5mo1•L-1时,可认为该离子沉淀完全,结合Ksp[Fe(OH)3]计算.
解答 解:(1)钴酸锂电池或锰酸锂电池中含有重金属离子,重金属离子会产生污染,所以磷酸铁锂电池比钴酸锂电池或锰酸锂电池更环保;
故答案为:磷酸铁锂电池不会产生重金属污染;
(2)①由原子守恒可知,Li2CO3+2FeC2O4•2H2O+2NH4H2PO4═2LiFePO4+2NH3↑+3CO2↑+2CO↑+7H2O↑;
故答案为:2CO↑、7H2O↑;
②C2O42-中C的化合价为+3价,生成CO和CO2,C元素的化合价分别为+2价、+3价,生成2molCO转移2mol电子,同时生成2molLiFePO4,则当反应中每转移0.15mol电子,生成0.15molLiFePO4,其质量为23.7g;
故答案为:23.7;
③亚铁离子容易被氧气氧化,所以要隔绝氧气,即反应需在惰性气氛的保护中进行;
故答案为:防止Fe(II)被氧化;
(3)电池工作时的总反应为:LiFePO4+6C$?_{放电}^{充电}$Li1-xFePO4+LixC6,放电时,Li1-xFePO4在正极上得电子发生还原反应,正极反应为Li1-xFePO4+xLi++xe-═LiFePO4;充电时,正极与外接电源的正极相连为阳极,阳离子向阴极移动,即Li+由左向右移动;电解质为锂盐,锂离子通过交换膜向正极移动,所以交换膜应该为阳离子交换膜;
故答案为:Li1-xFePO4+xLi++xe-═LiFePO4;由左向右;阳;
(4)②LiFePO4中亚铁离子在酸性条件下,被双氧水氧化为铁离子,则发生反应的离子方程式为2LiFePO4+2H++H2O2═2Li++2Fe3++2PO43-+2H2O;
故答案为:2LiFePO4+2H++H2O2═2Li++2Fe3++2PO43-+2H2O;
③当离子浓度小于l×10-5mo1•L-1时,可认为该离子沉淀完全,Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-),则c3(OH-)=$\frac{1×1{0}^{-39}}{1×1{0}^{-5}}$,所以c(OH-)=$\root{3}{0.1}$×10-11mol/L
≈0.464×10-11mol/L,则c(H+)=2.155×10-3mol/L,所以pH≈2.7;
故答案为:2.7.
点评 本题综合考查了物质的制备原理、原电池和电解池工作原理及相关计算,侧重于学生的分析能力和计算能力的考查,熟悉原电池、电解池工作原理及各个电极发生反应、明确溶度积数的表达式是解题关键,题目难度中等.

 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
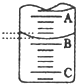
(2)如图表示50mL,滴定管中液面的位置,若A与C刻度间相差1mL,
A处的刻度为25,滴定管中液面读数应为25.40mL.,此时滴定管中液体的体积大于24.60mL.
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准漓浓度为c mol•L-1,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.32 | 25.28 |
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
E.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中总酸度的表达式(不必化简):$\frac{\frac{25.28+25.32}{2}×c×0.1×60}{2V}$.
| A. | W、X、Y、Z原子的核外最外层电子数的总和为19 | |
| B. | W的阴离子半径小于Li+ | |
| C. | W与Y可形成既含离子键又含共价键的化合物 | |
| D. | X、Y的简单气态氢化物的稳定性:X>Y |
| 选项 | 离子 | 要求 |
| A | K+、Cl-、SO42-、MnO4- | c(K+)<c(Cl-) |
| B | Na+、Ca2+、I-、NO3- | c(H+)/c(OH-)=1×1014 |
| C | Al3+、NH4+、SO42-、CH3COO- | 滴加NaOH溶液立刻有气体产生 |
| D | Na+、Mg2+、Ag+、NO3- | 滴加氨水先有沉淀产生,后沉淀部分溶解 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 用过量石灰乳吸收工业尾气中的SO2:Ca2++2OH-+SO2═CaSO3↑+H2O | |
| B. | 用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| C. | 用铜做电极电解NaCl溶液:2C1-+2H2O$\frac{\underline{\;高温\;}}{\;}$H2↑+Cl2↑+2OH- | |
| D. | 将Fe2O3加入到HI溶液中:Fe2O3+6H+═2Fe3++3H2O↑ |
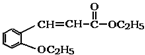 )是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,E为中间产物(结构简式为
)是合成高分子化合物M的单体,H可以通过有机物A(分子式为C7H8O)和丙酮为原料来进行合成,E为中间产物(结构简式为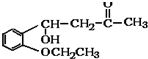 )其合成路线如图:
)其合成路线如图:
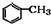 $→_{催化剂}^{O_{2}}$
$→_{催化剂}^{O_{2}}$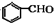
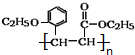 .
.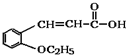 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$
 .
. .
.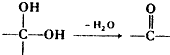
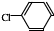 中氯原子较难水解
中氯原子较难水解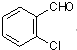 )可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
)可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式 、
、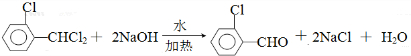 .该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式
.该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式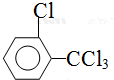 、
、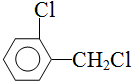 .
.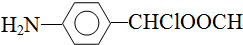 .
.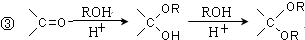
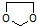 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: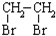
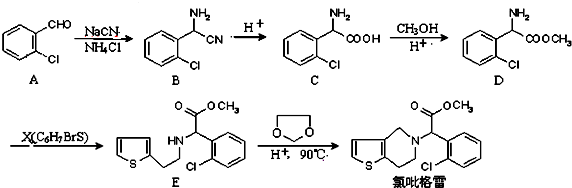
 )是临床上一种降脂抗血栓药物,它的一条合成路线如下:
)是临床上一种降脂抗血栓药物,它的一条合成路线如下:

 .
. .
.