题目内容
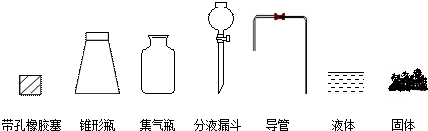
用如图装置进行铁粉在高温下与水蒸气反应的实验,请回答问题:
(1)装置A的作用是 ;
(2)装置B中发生的化学方程式为 ;
(3)干燥管C内盛放的药品是 ,能说明产生了H2的现象是 .

(1)装置A的作用是
(2)装置B中发生的化学方程式为
(3)干燥管C内盛放的药品是

考点:性质实验方案的设计,铁的化学性质
专题:
分析:由图可知,A中加热提供水蒸气,在B中发生Fe与水蒸气的反应生成四氧化三铁和氢气,C中干燥管干燥氢气,产生氢气的气泡,点燃肥皂泡可检验氢气,以此来解答.
解答:
解:(1)实验进行铁粉在高温下与水蒸气反应,则A的作用为提供水蒸气,故答案为:提供水蒸气;
(2)B中发生氧化还原反应:3Fe+4H2O
Fe3O4+4H2,故答案为:3Fe+4H2O
Fe3O4+4H2;
(3)C中药品为碱石灰,可干燥氢气,能说明产生了H2的现象是点燃肥皂泡,肥皂泡爆炸,故答案为:碱石灰;点燃肥皂泡,肥皂泡爆炸.
(2)B中发生氧化还原反应:3Fe+4H2O
| ||
| ||
(3)C中药品为碱石灰,可干燥氢气,能说明产生了H2的现象是点燃肥皂泡,肥皂泡爆炸,故答案为:碱石灰;点燃肥皂泡,肥皂泡爆炸.
点评:本题考查性质实验的设计,为高频考点,把握发生的反应及装置的作用为解答关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
 将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol?L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )
将氢氧化钠、氯化钡和硫酸铝三种固体组成的混合物溶于足量的水中,充分溶解,用1mol?L-1稀硫酸滴定,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )| A、A点所表示的沉淀是:Al(OH)3、BaSO4 |
| B、B-C段所发生反应的离子方程式是:H++OH-→H2O |
| C、A-B段发生反应的离子方程式:Ba2++SO42-→BaSO4↓ |
| D、拐点E的横坐标为70mL |
短周期主族元素X、Y、Z、W原子序数依次增大,已知Y是四种元素中金属性最强的元素,Y、Z、W同周期,且三种元素原子的最外层电子数之和为11,X2-和Y+具有相同的电子层结构,下列叙述正确的是( )
| A、离子半径:X2->Y+ |
| B、原子的最外层电子数:X>Y>Z>W |
| C、单质沸点:X>Y>Z>W |
| D、X与Y形成的化合物中只2含有离子键 |
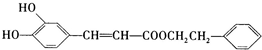 是一种天然抗癌药物,在一定条件下能发生如下转化:
是一种天然抗癌药物,在一定条件下能发生如下转化: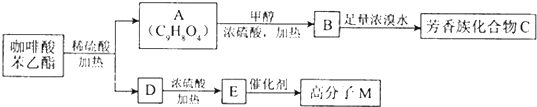
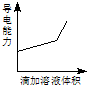 浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )