题目内容
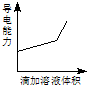 浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )| A | B | C | D | |
| 溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
| 溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |
| A、A | B、B | C、C | D、D |
考点:电解质溶液的导电性
专题:
分析:溶液导电能力的强弱主要取决于阴、阳离子浓度的大小,离子浓度越大,导电能力越强,以此分析.
解答:
解:A、浓度均为0.1mol/L的盐酸,滴加同浓度的氢氧化钠溶液,生成氯化钠,溶液的体积变大,导致浓度减小,导电能力减弱,故A错误;
B、醋酸是弱电解质部分电离,向其中滴入氢氧化钠,促进醋酸的电离,生成强电解质,自由移动离子浓度增大,导电能力增强,恰好完全反应后生成0.05mol/L的CH3COONa溶液,若此时继续滴加0.1mol/LNaOH溶液,溶液导电性增加更快,故B正确;
C、向氢氧化钠溶液中滴入氨水,碱性溶液中氨水的电离程度减小,自由移动离子的物质的量增加不明显,但溶液的体积变大,导电能力减弱,故C错误;
D、硝酸银溶液滴入氨水中,先产生白色沉淀,反应方程式为:AgNO3+NH3?H2O=AgOH+NH4NO3,完全反应后生成0.5mol/L的NH4NO3,继续滴加氨水沉淀消失AgOH+2NH3?H2O=[Ag(NH3)2]OH+2H2O,而[Ag(NH3)2]OH是一元强碱,但由于加入的氨水体积和生成[Ag(NH3)2]OH比例为2:1,因此导致导电能力不会有明显增强,故D错误;
故选B.
B、醋酸是弱电解质部分电离,向其中滴入氢氧化钠,促进醋酸的电离,生成强电解质,自由移动离子浓度增大,导电能力增强,恰好完全反应后生成0.05mol/L的CH3COONa溶液,若此时继续滴加0.1mol/LNaOH溶液,溶液导电性增加更快,故B正确;
C、向氢氧化钠溶液中滴入氨水,碱性溶液中氨水的电离程度减小,自由移动离子的物质的量增加不明显,但溶液的体积变大,导电能力减弱,故C错误;
D、硝酸银溶液滴入氨水中,先产生白色沉淀,反应方程式为:AgNO3+NH3?H2O=AgOH+NH4NO3,完全反应后生成0.5mol/L的NH4NO3,继续滴加氨水沉淀消失AgOH+2NH3?H2O=[Ag(NH3)2]OH+2H2O,而[Ag(NH3)2]OH是一元强碱,但由于加入的氨水体积和生成[Ag(NH3)2]OH比例为2:1,因此导致导电能力不会有明显增强,故D错误;
故选B.
点评:本题考查电解质溶液的导电性,题目难度中等,注意从离子反应的角度去分析电解质溶液阴、阳离子浓度的大小,离子浓度越大,导电能力越强.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
化学与生活息息相关,下列说法正确的是( )
| A、SO2、CO2和NO2都是可形成酸雨的气体 |
| B、棉、麻和油脂都是高分子化合物 |
| C、氧化铝陶瓷和光导纤维都是无机非金属材料 |
| D、纤维素在人体内可水解成葡萄糖,供人体组织的营养需要 |
下列关于电解质溶液中离子关系的说法正确的是( )
| A、0.1mol?L-1NaHCO3溶液中离子浓度关系:c(Na+)=2c(CO32-)+c(HCO3-)+c(H2CO3) |
| B、0.1mol?L-1NH4Cl和0.1mol?L-1NH3?H2O等体积混合后离子浓度关系:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、常温下,向醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中:c(Na+)=c(CH3COO-) |
| D、常温下,在pH=1的溶液中,Fe2+、NO3-、ClO-、Na+能大量共存 |
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)═N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图象作出的判断正确的是( )
A、 降低温度,平衡向正反应方向移动 |
B、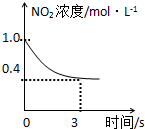 0-3s内,反应速率V (NO2)=0.2 mol?L-1 |
C、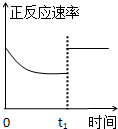 t1时仅加入催化剂,平衡正向移动 |
D、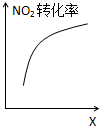 达到平衡时,仅改变X,则X为C(O2) |
下列叙述中,正确的是( )
| A、硅化学性质很稳定,因此硅在自然界中以游离态形式存在 |
| B、实验结束后,将废液倒入下水道排出实验室,以免污染实验室 |
| C、实验室盛装NaOH溶液的试剂瓶要用橡皮塞而不用玻璃塞 |
| D、向待测液先滴加新制氯水再滴加KSCN溶液,溶液变成血红色,说明待测液中一定有Fe2+ |