题目内容
15.在无色透明的酸性溶液中,能大量共存的离子组是( )| A. | Na+、K+、HCO3-、NO3- | B. | NH4+、Al3+、SO42-、NO3- | ||
| C. | K+、Fe2+、NH4+、NO3- | D. | NH4+、Na+、NO3-、OH- |
分析 无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,酸性溶液中存在大量氢离子,
A.碳酸氢根离子与氢离子反应生成二氧化碳气体和水;
B.四种离子之间不反应都不与氢离子反应,且为无色溶液;
C.亚铁离子为有色离子,且酸性条件下硝酸根离子能够氧化亚铁离子;
D.铵根离子、氢离子与氢氧根离子反应.
解答 解:酸性溶液中存在大量氢离子,溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.HCO3-与氢离子反应,在溶液中不能大量共存,故A错误;
B.NH4+、Al3+、SO42-、NO3-之间不发生反应,都是无色离子,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.Fe2+为有色离子,Fe2+、NO3-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.NH4+、H+都与OH-发生反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
5.向FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤沉淀,然后在空气中灼烧沉淀,最终得到的固体物质是( )
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)3 | D. | Fe3O4 |
6.“神舟”飞船成功发射,标志着我国航天科技达到了较高水平.为了降低宇航员所在轨道舱和返回舱内二氧化碳的浓度,同时释放氧气,舱内放入下列哪种物质能满足上述要求( )
| A. | H2O | B. | Na2O2 | C. | KClO3 | D. | KMnO4 |
10.下列叙述正确的是( )
| A. | 某溶液的pH=7,则该溶液为中性溶液 | |
| B. | 一定温度下,向AgCl饱和溶液中加入少量NaCl固体,Ksp(AgCl)减小 | |
| C. | 常温下,反应X(s)+Y(l)═2Z(g)不能自发,则该反应的△H>0 | |
| D. | 常温下,0.01mol/L的NaOH溶液中由水电离的c(H+)=1.0×10-2mol/L |
7.将浓氨水分别滴加到下列4种溶液中,下列说法不正确的是( )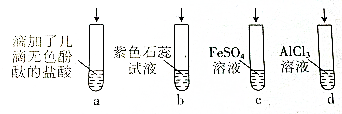

| A. | 若滴加过量的浓氨水,试管a中溶液由无色变红色 | |
| B. | 试管b中溶液由紫色变为蓝色 | |
| C. | 试管c中先有白色沉淀,后变为灰绿色,然后变为红褐色 | |
| D. | 试管d中先有白色沉淀,后白色沉淀消失 |
