题目内容
7.将浓氨水分别滴加到下列4种溶液中,下列说法不正确的是( )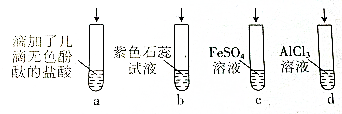
| A. | 若滴加过量的浓氨水,试管a中溶液由无色变红色 | |
| B. | 试管b中溶液由紫色变为蓝色 | |
| C. | 试管c中先有白色沉淀,后变为灰绿色,然后变为红褐色 | |
| D. | 试管d中先有白色沉淀,后白色沉淀消失 |
分析 A.酚酞在碱性溶液中呈红色,在酸性溶液中呈无色,一水合氨为碱能够与盐酸发生酸性中和反应;
B.氨水中含有一水合氨,一水合氨部分电离生成氢氧根离子,溶液显碱性;
C.氨水与硫酸亚铁反应生成氢氧化亚铁,氢氧化亚铁不稳定,继续氧化为氢氧化铁;
D.氢氧化铝只能溶解在强碱中.
解答 解:A.盐酸加酚酞溶液为无色,逐滴滴加氨水直到过量,氨水中的一水合氨为碱能够与盐酸发生酸性中和反应,溶液由酸性变为碱性,所以溶液由无色变红色,故A正确;
B.氨水中含有一水合氨,一水合氨部分电离生成氢氧根离子,溶液显碱性,能够使紫色石蕊变蓝,故B正确;
C.氨水与硫酸亚铁反应生成氢氧化亚铁,氢氧化亚铁不稳定,继续氧化为氢氧化铁,现象为先有白色沉淀,后变为灰绿色,然后变为红褐色,故C正确;
D.氨水中的一水合氨为弱碱,与氯化铝反应生成氢氧化铝沉淀,氢氧化铝不溶于氨水,所以现象产生白色沉淀,沉淀不消失,故D错误;
故选:D.
点评 本题考查了实验现象的判断,明确氨水的成分及性质是解题关键,题目难度不大.

练习册系列答案
相关题目
18.常温下,将0.40mol/L氢氧化钠溶液与0.10mol/L硫酸溶液等体积混合,该混合溶液的pH为( )
| A. | 1.0 | B. | 2.0 | C. | 13.0 | D. | 14.0 |
15.在无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Na+、K+、HCO3-、NO3- | B. | NH4+、Al3+、SO42-、NO3- | ||
| C. | K+、Fe2+、NH4+、NO3- | D. | NH4+、Na+、NO3-、OH- |
12.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制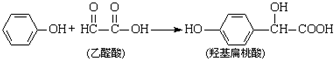
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 该反应是取代反应 | |
| B. | 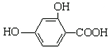 和羟基扁桃酸互为同系物 和羟基扁桃酸互为同系物 | |
| C. | 1个烃基扁桃酸分子中最多有17个原子共平面 | |
| D. | 1mol羟基扁桃酸分子最多能分别和1mol NaHCO3、2mol Na0H、3mol Na、4mol H2发生反应 |
4.我国采用长征三号甲运载火箭成功发射了“嫦娥一号”卫星.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气.已知:
N2(g)+2O2(g)═N2O4(g)△H=+8.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
N2(g)+2O2(g)═N2O4(g)△H=+8.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
| A. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1076.7 kJ/mol | |
| B. | N2H4(g)+$\frac{1}{2}$N2O4(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=-542.7 kJ/mol | |
| C. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-542.7 kJ/mol | |
| D. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(l)△H=-1059.3 kJ/mol |
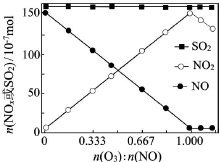 烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量.O3氧化烟气中SO2、NOx的主要反应的热化学方程式为: