题目内容
洪水过后,灾区供水设施及饮用井水受污染;赤脚医生挨家挨户发放两包白色固体:漂白粉和明矾.
(1)漂白粉的作用是 ;
(2)明矾的作用是 ,说出其三大理由中的至少两大理由 .
(3)甲同学认为漂白粉、明矾不能同时加入水中,否则效果不理想,其理由是(写离子方程式即可) .但乙同学认为混用效果更佳,理由是 .
(4)请你设计一个实验来证明这两种观点谁正确 .
(1)漂白粉的作用是
(2)明矾的作用是
(3)甲同学认为漂白粉、明矾不能同时加入水中,否则效果不理想,其理由是(写离子方程式即可)
(4)请你设计一个实验来证明这两种观点谁正确
考点:性质实验方案的设计,氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:(1)漂白粉可用于杀菌消毒;
(2)明矾可水解生成具有吸附性的氢氧化铝胶体;
(3)明矾水解显酸性,漂白粉水解呈碱性,发生互促水解反应;
(4)可从氧化性和净水的角度设计实验.
(2)明矾可水解生成具有吸附性的氢氧化铝胶体;
(3)明矾水解显酸性,漂白粉水解呈碱性,发生互促水解反应;
(4)可从氧化性和净水的角度设计实验.
解答:
解:(1)漂白粉可生成具有强氧化性的次氯酸,可用于杀菌消毒,故答案为:杀菌消毒;
(2)明矾可水解生成具有吸附性的氢氧化铝胶体,可用于净水,原因是①明矾是电解质,加入电解质可以使水中的胶态杂质聚沉;②明矾水解产生的Al(OH)3胶体的胶粒带正电与水中的硅酸溶胶的胶粒(带负电)发生电中和而聚沉;③Al(OH)3胶体可以吸附水中悬浮的碱性杂质,
故答案为:净水;①明矾是电解质,加入电解质可以使水中的胶态杂质聚沉;②明矾水解产生的Al(OH)3胶体的胶粒带正电与水中的硅酸溶胶的胶粒(带负电)发生电中和而聚沉;③Al(OH)3胶体可以吸附水中悬浮的碱性杂质;
(3)明矾水解显酸性,漂白粉水解呈碱性,发生互促水解反应,反应的离子方程式为Al3++3ClO-+3H2O=Al(OH)3↓+3HClO,
乙同学认为混用效果更佳,可能认为产生更多Al(OH)3和HClO,
故答案为:Al3++3ClO-+3H2O=Al(OH)3↓+3HClO;明矾水解显酸性,漂白粉水解呈碱性,两者混用,相互促进,产生更多Al(OH)3和HClO,而这正是明矾净水及漂白粉杀菌消毒所需要的.
(4)可从氧化性和净水的角度设计实验:
将2ag漂白粉和2bg明矾混合均匀,形成固体混合物,均分成两等份.①取ag漂白粉和1份固体混合物分别投入盛等量品红溶液的烧杯中,看其褪色的快慢程度;②取bg明矾和另一份固体混合物分别投入盛等量泥水的两个烧杯中,看泥水澄清的快慢程度,
故答案为:将2ag漂白粉和2bg明矾混合均匀,形成固体混合物,均分成两等份.①取ag漂白粉和1份固体混合物分别投入盛等量品红溶液的烧杯中,看其褪色的快慢程度;②取bg明矾和另一份固体混合物分别投入盛等量泥水的两个烧杯中,看泥水澄清的快慢程度.
(2)明矾可水解生成具有吸附性的氢氧化铝胶体,可用于净水,原因是①明矾是电解质,加入电解质可以使水中的胶态杂质聚沉;②明矾水解产生的Al(OH)3胶体的胶粒带正电与水中的硅酸溶胶的胶粒(带负电)发生电中和而聚沉;③Al(OH)3胶体可以吸附水中悬浮的碱性杂质,
故答案为:净水;①明矾是电解质,加入电解质可以使水中的胶态杂质聚沉;②明矾水解产生的Al(OH)3胶体的胶粒带正电与水中的硅酸溶胶的胶粒(带负电)发生电中和而聚沉;③Al(OH)3胶体可以吸附水中悬浮的碱性杂质;
(3)明矾水解显酸性,漂白粉水解呈碱性,发生互促水解反应,反应的离子方程式为Al3++3ClO-+3H2O=Al(OH)3↓+3HClO,
乙同学认为混用效果更佳,可能认为产生更多Al(OH)3和HClO,
故答案为:Al3++3ClO-+3H2O=Al(OH)3↓+3HClO;明矾水解显酸性,漂白粉水解呈碱性,两者混用,相互促进,产生更多Al(OH)3和HClO,而这正是明矾净水及漂白粉杀菌消毒所需要的.
(4)可从氧化性和净水的角度设计实验:
将2ag漂白粉和2bg明矾混合均匀,形成固体混合物,均分成两等份.①取ag漂白粉和1份固体混合物分别投入盛等量品红溶液的烧杯中,看其褪色的快慢程度;②取bg明矾和另一份固体混合物分别投入盛等量泥水的两个烧杯中,看泥水澄清的快慢程度,
故答案为:将2ag漂白粉和2bg明矾混合均匀,形成固体混合物,均分成两等份.①取ag漂白粉和1份固体混合物分别投入盛等量品红溶液的烧杯中,看其褪色的快慢程度;②取bg明矾和另一份固体混合物分别投入盛等量泥水的两个烧杯中,看泥水澄清的快慢程度.
点评:本题考查较为综合,设计实验方案的设计、物质的性质及应用,侧重于学生的分析能力和实验能力的考查,注意把握实验的角度以及物质的性质的异同,难度中等.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
下列表述不正确的是( )
| A、常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 |
| B、NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中阴离子只有CO32-和OH- |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中,c(Na+)=c(CH3COO-) |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、16g O3与16g O2含有相同的氧原子数 |
| B、2.3g Na+中含有的电子数为0.1NA |
| C、1mol O2所含的原子数为NA |
| D、2.4g镁变为Mg2+时失去的电子数为0.1NA |
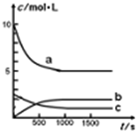 一定温度下,在体积为1L的恒容密闭容器中充入10mol NO2和2.5molO2发生反应:4NO2(g)+O2(g)?2N2O5(g)△H<0.反应混合物中NO2和物质的量浓度随时间的变化如表所示:
一定温度下,在体积为1L的恒容密闭容器中充入10mol NO2和2.5molO2发生反应:4NO2(g)+O2(g)?2N2O5(g)△H<0.反应混合物中NO2和物质的量浓度随时间的变化如表所示: 系统命名为
系统命名为