题目内容
已知氨气可以和氯气发生如下反应:8NH3+3Cl2=6NH4Cl+N2 回答下列问题:
(1)该反应中的氧化剂和还原产物分别是 , .
(2)在反应中若有28g N2 生成,被氧化的氨有 g..
(1)该反应中的氧化剂和还原产物分别是
(2)在反应中若有28g N2 生成,被氧化的氨有
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应8NH3+3Cl2=6NH4Cl+N2 中Cl元素化合价由0价变为-1价、N元素化合价由-3价变为0价,所以氯气是氧化剂,氯化铵是还原产物,根据氮原子守恒计算被氧化的氨气质量.
解答:
解:(1)该反应8NH3+3Cl2=6 NH4Cl+N2 中Cl元素化合价由0价变为-1价、N元素化合价由-3价变为0价,所以氯气是氧化剂、部分氨气是还原剂,氯化铵是还原产物、氮气是氧化产物,故答案为:Cl2;NH4Cl;
(2)如果反应中有28g N2 生成,n(N2)=
=1mol,根据氮原子守恒知,被氧化的氨气的物质的量为2mol,其质量=2mol×17g/mol=34g,故答案为:34.
(2)如果反应中有28g N2 生成,n(N2)=
| 28g |
| 28g/mol |
点评:本题考查了氧化还原反应,明确元素化合价变化是解本题关键,结合基本概念来分析解答,注意(2)采用原子守恒即可解答,注意只有部分氨气作还原剂,为易错点.

练习册系列答案
相关题目
下列各组元素中,按最高正价递增顺序排列的是( )
| A、C、N、O |
| B、Li、Na、K |
| C、Cl、Br、I |
| D、Na、Mg、Al |
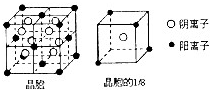 A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的.
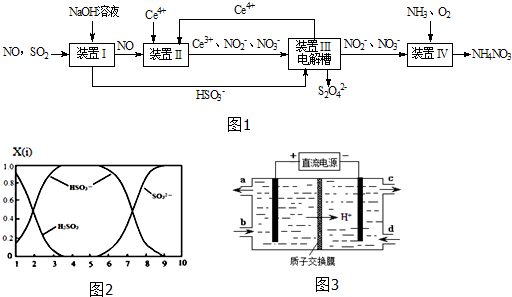
A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的.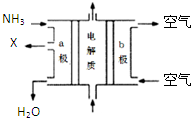 工业废水中含有多种有害成分,任意排放将造成严重污染,进行分类处理达标后才能排放.
工业废水中含有多种有害成分,任意排放将造成严重污染,进行分类处理达标后才能排放.