题目内容
一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.25 mol?L-1?s-1 |
| B、12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的1/5 |
| C、若增大X的浓度,则物质Y的转化率减小 |
| D、若该反应的△H<0,升高温度,平衡常数K减小 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:经12s达到平衡,正反应速率等于逆反应速率,达到平衡之后,如外界条件不不变,则平衡状态不变,正逆反应速率相等,结合生成Z的物质的量进行相关的计算.
解答:
解:X(g)+3Y(g)?2Z(g)
起始量(mol) 1 3 0
转化量(mol)0.3 0.9 0.6
平衡量(mol)0.7 2.1 0.6
A、c(X)=
=0.0125mol(L?s),故A错误;
B、容器体积扩大至10L,平衡不移动时,Z的浓度是原来的
,但容器体积扩大时,平衡逆向移动,Z的浓度应小于原来的
,故B错误;
C、增大X的浓度,的质量增大,故C错误;
D、对放热反应升温时,平衡逆向移动,K减小,故D正确;
故选D.
起始量(mol) 1 3 0
转化量(mol)0.3 0.9 0.6
平衡量(mol)0.7 2.1 0.6
A、c(X)=
| ||
| 12s |
B、容器体积扩大至10L,平衡不移动时,Z的浓度是原来的
| 1 |
| 5 |
| 1 |
| 5 |
C、增大X的浓度,的质量增大,故C错误;
D、对放热反应升温时,平衡逆向移动,K减小,故D正确;
故选D.
点评:本题考查化学平衡问题,题目难度不大,本题注意外界条件对化学平衡的影响.

练习册系列答案
相关题目
下列有关金属及其化合物的说法中,错误的是( )
| A、生活中用碱液洗涤铝制饮具 |
| B、铁、铜制品要保持干燥,以防生锈 |
| C、用过氧化钠做潜水呼吸面具供氧剂 |
| D、用小苏打治疗胃酸过多 |
在2A+B?3C+4D中,表示该反应速率最快的是( )
| A、υ(A)=0.5mol?L-1?S-1 |
| B、υ(B)=0.3 mol?L-1?S-1 |
| C、υ(C)=0.8mol?L-1?S-1 |
| D、υ(D)=1 mol?L-1?S-1 |
如图有关电化学的示意图正确的是( )
A、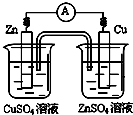 |
B、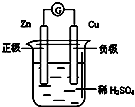 |
C、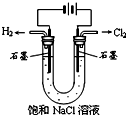 |
D、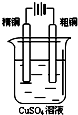 |
2007年国家最高科学技术奖授予石油化工催化剂专家闵恩泽教授,以表彰他在催化剂研究方面做出的突出贡献.下列关于催化剂的说法正确的是( )
| A、使用催化剂可以增大正反应速率,减小逆反应速率 |
| B、使用催化剂可以使化学平衡向正反应方向移动 |
| C、使用催化剂可以降低反应的活化能 |
| D、使用催化剂可以改变反应的平衡常数 |
下列化学式中,能表示正长石(KAlSi3O8)的是( )
| A、K2O?Al2O3?3SiO2 |
| B、K2O?2Al2O3?3SiO2 |
| C、K2O?Al2O3?6SiO2 |
| D、2K2O?2Al2O3?6SiO2 |
下列关于氧化还原反应的说法正确的是( )
| A、氧化还原反应中,发生氧化还原的一定是不同种元素 |
| B、氧化剂和还原剂一定是不同种物质 |
| C、还原剂失去电子总数一定等于氧化剂得到电子总数 |
| D、某氧化还原反应中,还原剂共失去4e-,氧化剂共得到4e-,所以该反应转移的电子总数为8e- |
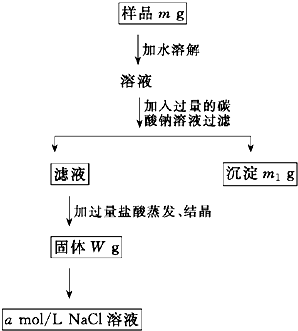 欲用含有少量氯化钙的氯化钠固体,配制100mL a mol/L的氯化钠溶液,设计了下面的操作方案.根据方案操作步骤回答下列问题:
欲用含有少量氯化钙的氯化钠固体,配制100mL a mol/L的氯化钠溶液,设计了下面的操作方案.根据方案操作步骤回答下列问题: