题目内容
2007年国家最高科学技术奖授予石油化工催化剂专家闵恩泽教授,以表彰他在催化剂研究方面做出的突出贡献.下列关于催化剂的说法正确的是( )
| A、使用催化剂可以增大正反应速率,减小逆反应速率 |
| B、使用催化剂可以使化学平衡向正反应方向移动 |
| C、使用催化剂可以降低反应的活化能 |
| D、使用催化剂可以改变反应的平衡常数 |
考点:催化剂的作用
专题:
分析:催化剂在化学反应前后质量和化学性质保持不变,可以能降低反应的活化能加快化学反应速率,但是不会引起化学平衡的移动,据此分析.
解答:
解:A、使用催化剂可以同等程度的增大正逆反应速率,故A错误;
B、使用催化剂可以改变速率,但是不会引起化学平衡的移动,故B错误;
C、使用催化剂可以降低反应的活化能,从而加快化学反应速率,故C正确;
D、使用催化剂可以使反应的速率加快,但是平衡不移动,不会引起平衡常数的改变,故D错误.
故选C.
B、使用催化剂可以改变速率,但是不会引起化学平衡的移动,故B错误;
C、使用催化剂可以降低反应的活化能,从而加快化学反应速率,故C正确;
D、使用催化剂可以使反应的速率加快,但是平衡不移动,不会引起平衡常数的改变,故D错误.
故选C.
点评:本题考查了催化剂对活化能、反应速率和化学平衡的影响,题目难度不大,注意把握催化剂的含义以及对反应的影响.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
Mg(OH)2在下列四种情况下,其溶解度最大的是( )
| A、在纯水中 |
| B、在0.1 mol?L-1的CH3COOH溶液中 |
| C、在0.1 mol?L-1的NH3?H2O溶液中 |
| D、在0.1 mol?L-1的MgCl2溶液中 |
已知某酸H2B在水溶液中存在下列关系:①H2B?H++HB-,②HB-?H++B2-.关于该酸对应的酸式盐NaHB的溶液,
下列说法中一定正确的是( )
下列说法中一定正确的是( )
| A、NaHB属于弱电解质 |
| B、溶液中的离子浓度c(Na+)>c(HB-)>c(H+)>c(OH-) |
| C、c(Na+)=c(HB-)+c(B2-)+c(H2B) |
| D、NaHB和NaOH溶液反应的离子方程式为H++OH-=H2O |
一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.25 mol?L-1?s-1 |
| B、12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的1/5 |
| C、若增大X的浓度,则物质Y的转化率减小 |
| D、若该反应的△H<0,升高温度,平衡常数K减小 |
往含有H+、Fe2+、Cu2+、Ag+四种离子的溶液中加入足量镁粉,最先得到的还原产物是( )
| A、H2 | B、Fe |
| C、Cu | D、Ag |
强酸与强碱的稀溶液发生中和反应的热化学方程式为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,分别向1L 0.5mol/L的NaOH溶液中加入:①稀醋酸;②浓H2SO4;③稀硝酸.恰好完全反应时的热效应分别为△H1、△H2、△H3,它们的关系正确的是( )
| A、△H1>△H2>△H3 |
| B、△H2>△H3>△H1 |
| C、△H1=△H2=△H3 |
| D、△H1>△H3>△H2 |
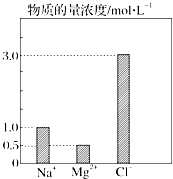 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示.
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示.