题目内容
下列有关金属及其化合物的说法中,错误的是( )
| A、生活中用碱液洗涤铝制饮具 |
| B、铁、铜制品要保持干燥,以防生锈 |
| C、用过氧化钠做潜水呼吸面具供氧剂 |
| D、用小苏打治疗胃酸过多 |
考点:钠的重要化合物,铝的化学性质
专题:几种重要的金属及其化合物
分析:A、铝制品表面的氧化铝是两性氧化物和酸碱发生反应;
B、铁、铜在潮湿空气中发生电化腐蚀生锈;
C、过氧化钠可以与二氧化碳反应生成碳酸钠和氧气;
D、小苏打是碳酸氢钠可以用来治疗胃酸过多;
B、铁、铜在潮湿空气中发生电化腐蚀生锈;
C、过氧化钠可以与二氧化碳反应生成碳酸钠和氧气;
D、小苏打是碳酸氢钠可以用来治疗胃酸过多;
解答:
解:A、铝制品表面的氧化铝是两性氧化物和酸碱发生反应,不能用碱液洗涤铝制饮具,故A错误;
B、铁、铜在潮湿空气中发生电化腐蚀生锈,铁、铜制品应要保持干燥,以防生锈,故B正确;
C、过氧化钠可以与二氧化碳反应生成碳酸钠和氧气,做潜水呼吸面具供氧剂,故C正确;
D、小苏打是碳酸氢钠和胃酸中盐酸反应,可以用来治疗胃酸过多,故D正确;
故选A.
B、铁、铜在潮湿空气中发生电化腐蚀生锈,铁、铜制品应要保持干燥,以防生锈,故B正确;
C、过氧化钠可以与二氧化碳反应生成碳酸钠和氧气,做潜水呼吸面具供氧剂,故C正确;
D、小苏打是碳酸氢钠和胃酸中盐酸反应,可以用来治疗胃酸过多,故D正确;
故选A.
点评:本题考查了化学与生活的理解应用,主要是物质俗称,性质的分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
下列图示实验正确的是( )
A、 碳酸氢钠受热分解 |
B、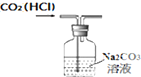 除去CO2中HCl |
C、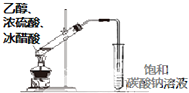 制备乙酸乙酯 |
D、 制备收集干燥的氨气 |
足量下列物质与等质量的铝反应,放出氢气且消耗溶质物质的量最少的是( )
| A、氢氧化钠溶液 | B、稀硫酸 |
| C、盐酸 | D、水 |
等质量铝镁合金粉末分别与下列四种过量的物质充分反应,放出氢气最多的是( )
| A、NaOH溶液 |
| B、H2SO4溶液 |
| C、蔗糖溶液 |
| D、NaCl溶液 |
Mg(OH)2在下列四种情况下,其溶解度最大的是( )
| A、在纯水中 |
| B、在0.1 mol?L-1的CH3COOH溶液中 |
| C、在0.1 mol?L-1的NH3?H2O溶液中 |
| D、在0.1 mol?L-1的MgCl2溶液中 |
一小块钠暴露在空气中一段时间,发生的反应是( )
①4Na+O2=2Na2O
②2Na+O2=Na2O2
③Na2O+H2O=2NaOH
④2NaOH+CO2=Na2CO3+H2O.
①4Na+O2=2Na2O
②2Na+O2=Na2O2
③Na2O+H2O=2NaOH
④2NaOH+CO2=Na2CO3+H2O.
| A、① | B、②④ | C、①③ | D、①③④ |
一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.25 mol?L-1?s-1 |
| B、12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的1/5 |
| C、若增大X的浓度,则物质Y的转化率减小 |
| D、若该反应的△H<0,升高温度,平衡常数K减小 |
 如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得两个装置中均通过0.02mol电子时(不考虑盐的水解和溶液体积的变化)则下列叙述中正确的是( )
如右图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得两个装置中均通过0.02mol电子时(不考虑盐的水解和溶液体积的变化)则下列叙述中正确的是( )| A、电极上析出物质的质量:①=② |
| B、溶液的pH变化:①增大,②不变 |
| C、电极反应式:①中阳极 2Cl--2e-═Cl2↑ ②中负极 2H++2e-═H2↑ |
| D、产生气体的体积:①=② |