题目内容
如图有关电化学的示意图正确的是( )
A、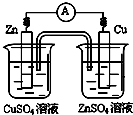 |
B、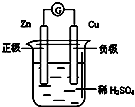 |
C、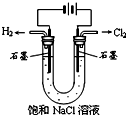 |
D、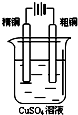 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.含有盐桥的原电池中,电极材料和电解质溶液中阳离子元素必须相同;
B.该原电池中,Zn易失电子作负极、Cu作正极;
C.该电解池中,阳极上氯离子放电、阴极上氢离子放电;
D.电解精炼粗铜时,粗铜作阳极、纯铜作阴极.
B.该原电池中,Zn易失电子作负极、Cu作正极;
C.该电解池中,阳极上氯离子放电、阴极上氢离子放电;
D.电解精炼粗铜时,粗铜作阳极、纯铜作阴极.
解答:
解:A.含有盐桥的原电池中,电极材料和电解质溶液中阳离子元素必须相同,所以Cu电极必须插入硫酸铜溶液中、Zn电极必须插入硫酸锌溶液中,故A错误;
B.该原电池中,Zn易失电子作负极、Cu作正极,正极上氢离子放电,故B错误;
C.该电解池中,阳极上氯离子放电、阴极上氢离子放电,所以阳极上生成氯气、阴极上生成氢气,故C正确;
D.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,阳极上粗铜失电子发生氧化反应,阴极上铜离子得电子发生还原反应,故D错误;
故选C.
B.该原电池中,Zn易失电子作负极、Cu作正极,正极上氢离子放电,故B错误;
C.该电解池中,阳极上氯离子放电、阴极上氢离子放电,所以阳极上生成氯气、阴极上生成氢气,故C正确;
D.电解精炼粗铜时,粗铜作阳极、纯铜作阴极,阳极上粗铜失电子发生氧化反应,阴极上铜离子得电子发生还原反应,故D错误;
故选C.
点评:本题考查原电池和电解池原理,明确原电池正负极的判断方法、电解池中离子放电顺序即可解答,知道盐桥的作用及盐桥中阴阳离子移动方向.

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
等质量铝镁合金粉末分别与下列四种过量的物质充分反应,放出氢气最多的是( )
| A、NaOH溶液 |
| B、H2SO4溶液 |
| C、蔗糖溶液 |
| D、NaCl溶液 |
一小块钠暴露在空气中一段时间,发生的反应是( )
①4Na+O2=2Na2O
②2Na+O2=Na2O2
③Na2O+H2O=2NaOH
④2NaOH+CO2=Na2CO3+H2O.
①4Na+O2=2Na2O
②2Na+O2=Na2O2
③Na2O+H2O=2NaOH
④2NaOH+CO2=Na2CO3+H2O.
| A、① | B、②④ | C、①③ | D、①③④ |
下列各组离子在水溶液中能大量共存的是( )
| A、Na+、HS-、Cu2+、Cl- |
| B、HCO3-、Na+、OH-、K+ |
| C、K+、CO32-、Br-、AlO2- |
| D、H+、K+、Cl-、SO32- |
一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.25 mol?L-1?s-1 |
| B、12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的1/5 |
| C、若增大X的浓度,则物质Y的转化率减小 |
| D、若该反应的△H<0,升高温度,平衡常数K减小 |
下列叙述错误的是( )
| A、铜锌合金制成的假金元宝欺骗行人的事件屡有发生,可以把它放入硝酸中进行鉴别 |
| B、装饰材料中的甲醛、芳香烃及氡等会造成居室污染 |
| C、绿色食品是不含任何化学物质的食品 |
| D、塑料的主要成分是合成树脂,有的塑料可以能导电 |
在反应3BrF3+5H2O=HBrO3+9HF+O2↑+Br2中当有45g水被氧化时,被水还原的BrF3的物质的量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
