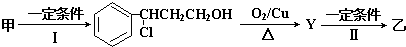题目内容
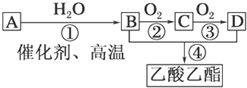 根据所给信息填空
根据所给信息填空已知:①A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2
| 催化剂 |
| △ |
(1)A、B、C、D中所有原子都在同一平面上的是
(2)写出下列反应的反应类型:①
(3)B、D的结构简式
考点:有机物的推断
专题:
分析:A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应得到B为CH3CH2OH,B能氧化得到C为CH3CHO,C氧化得到D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯,据此解答.
解答:
解:A的产量通常用来衡量一个国家的石油化工水平,则A为CH2=CH2,乙烯与水发生加成反应得到B为CH3CH2OH,B能氧化得到C为CH3CHO,C氧化得到D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯,
(1)A、B、C、D中乙烯为平面结构,所以原子都在同一平面内,其它物质分子存在甲基,具有甲烷的四面体结构,所有原子不可能在同一平面上,故答案为:A;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应④是乙醇与乙酸发生酯化反应生成乙酸乙酯,
故答案为:加成反应;酯化反应;
(3)由上述分析可知,B的结构简式为CH3CH2OH、D的结构简式为CH3COOH,故答案为:CH3CH2OH;CH3COOH.
(1)A、B、C、D中乙烯为平面结构,所以原子都在同一平面内,其它物质分子存在甲基,具有甲烷的四面体结构,所有原子不可能在同一平面上,故答案为:A;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应④是乙醇与乙酸发生酯化反应生成乙酸乙酯,
故答案为:加成反应;酯化反应;
(3)由上述分析可知,B的结构简式为CH3CH2OH、D的结构简式为CH3COOH,故答案为:CH3CH2OH;CH3COOH.
点评:本题考查无机物推断,涉及烯烃、醇、醛、羧酸的性质与转化,比较基础,侧重对基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
根据下列化学方程式,判断有关物质的还原性强弱的顺序为( )
①I2+SO2+2H2O═H2SO4+2HI;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2.
①I2+SO2+2H2O═H2SO4+2HI;
②2FeCl2+Cl2═2FeCl3;
③2FeCl3+2HI═2FeCl2+2HCl+I2.
| A、I->Fe2+>Cl->SO2 |
| B、Cl->Fe2+>SO2>I- |
| C、Fe2+>I->Cl->SO2 |
| D、SO2>I->Fe2+>Cl- |
已知反应①:CO(g)+CuO(s)?CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)?Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)?CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是( )
A、反应①的平衡常数K1=
| ||
B、反应③的平衡常数K=
| ||
| C、对于反应③,恒容时,温度升高,H2浓度减小,则该反应的△H>0 | ||
| D、对于反应③,恒温恒容下,增大压强,H2浓度一定减小 |
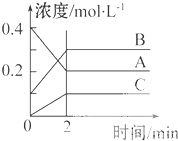 如图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )
如图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )| A、发生的反应可表示为:2A(g)?2B(g)+C(g) |
| B、前2 min A的分解速率为0.1mol?L-1?min-1 |
| C、开始时,正逆反应同时开始 |
| D、2 min时,A、B、C的浓度之比为2:3:1 |
在一定条件下,向2L密闭容器中充入3mol X气体和1mol Y气体,发生下列反应:2X(g)+Y(g)?3Z(g)+2W(g),在某一时刻达到化学平衡时,测出的下列各生成物的物质的量的数据肯定错误的是( )
| A、n(Z)=1.5 mol |
| B、n(Z)=2.4 mol |
| C、n(W)=1.6 mol |
| D、n(W)=2.0 mol |
 使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.
使用酸碱中和滴定法测定某未知物质的量浓度的稀盐酸.