题目内容
在一定条件下,向2L密闭容器中充入3mol X气体和1mol Y气体,发生下列反应:2X(g)+Y(g)?3Z(g)+2W(g),在某一时刻达到化学平衡时,测出的下列各生成物的物质的量的数据肯定错误的是( )
| A、n(Z)=1.5 mol |
| B、n(Z)=2.4 mol |
| C、n(W)=1.6 mol |
| D、n(W)=2.0 mol |
考点:化学平衡建立的过程
专题:
分析:根据可逆反应的特点,反应物不可能在反应中完全转化,由于反应中X、Y按照物质的量2:1反应,所以X过量,利用极限法计算各物质的浓度来判断.
解答:
解:可逆反应中,反应物不可能在反应中完全转化,由于反应中X、Y按照物质的量2:1反应,所以X过量1mol,生成3molZ,2molW,但反应不可能完全进行到底,所以0<C(Z)<3mol/L;0<C(W)<2mol/L,只有D不在范围内,
故选D.
故选D.
点评:本题考查了可逆反应的特点,注意可逆反应中,反应物的转化率不可能是100%,利用极限法计算.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、含有NA个氦原子的氦气在标准状况下的体积约为11.2 L |
| B、在常温常压下,11.2 L Cl2含有的分子数约为0.5 NA |
| C、25℃,1.01×105Pa,64 g SO2中含有的原子数为3 NA |
| D、标准状况下,11.2 L H2O含有的分子数为0.5 NA |
下列有关说法正确的是( )
| A、若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| B、2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H<0 |
| C、增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
| D、对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
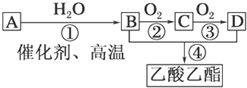 根据所给信息填空
根据所给信息填空