题目内容
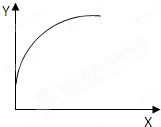 在一恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:2A(g)+B(g)?2C(g);△H<0.当达到平衡后,保持其他条件不变,只改变条件X,则相应量Y的改变一定符合图中曲线的是( )
在一恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:2A(g)+B(g)?2C(g);△H<0.当达到平衡后,保持其他条件不变,只改变条件X,则相应量Y的改变一定符合图中曲线的是( )| X | Y | |
| A | 温度 | C的体积分数 |
| B | 充入稀有气体 | A的物质的量 |
| C | 再加入A | B的转化率 |
| D | 再加入C | A的百分含量 |
| A、A | B、B | C、C | D、D |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:反应的特征是反应气体的化学计量数大于生成气体的化学计量数,则增大压强,平衡正向移动,该反应是放热反应,温度升高时化学平衡逆向移动,图象中纵坐标随横坐标的增大而增大,结合影响化学反应速率的因素解答该题.
解答:
解:A.该反应是放热反应,温度升高时化学平衡逆向移动,C的体积分数下降,与图不符合,故A错误;
B.恒容密闭容器中充入稀有气体,平衡不移动,A的物质的量不变,不符合,故B错误;
C.再加入A,平衡正向移动,B的转化率增大,符合,故C正确;
D.再加入C,相当于压强增大,平衡正向移动,A的百分含量减少,故D错误.
故选C.
B.恒容密闭容器中充入稀有气体,平衡不移动,A的物质的量不变,不符合,故B错误;
C.再加入A,平衡正向移动,B的转化率增大,符合,故C正确;
D.再加入C,相当于压强增大,平衡正向移动,A的百分含量减少,故D错误.
故选C.
点评:本题考查化学平衡的影响,为高频考点,侧重于学生的分析能力的考查,注意把握反应的特点以及题给信息,为解答该题的关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列反应中,不属于加成反应的是( )
| A、.乙炔与与氯化氢反应制取氯乙烯 |
| B、乙烷和氯气反应制取氯乙烷 |
| C、.乙烯与氢气反应制取乙烷 |
| D、.乙烯通入溴水,溴水褪色 |
由K2SO4、Al2(SO4)3 和Na2SO4 组成的混合溶液,c(Na+)=0.1mol/L,c(Al3+)=0.4mol/L,c(SO42-)=0.8mol/L,则 c(K+)为( )
| A、0.15 mol/L |
| B、0.2 mol/L |
| C、0.3 mol/L |
| D、0.4mol/L |
对可逆反应2SO2+O2
2SO3,下列叙述正确的是( )
| 催化剂 |
| △ |
| A、反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(SO2):n(O2)=2:1 |
| B、反应达到平衡后,缩小容器体积,正反应速率加快,逆反应速率减慢,平衡正向移动 |
| C、反应达到平衡时,加入催化剂,速率加快,平衡常数增大 |
| D、当v正(SO2):v正(SO3)=1:1时,说明该化学反应已经达到平衡 |
工业上用洗净的废铜作原料来制备硝酸铜.为了节约原料和防止污染环境,宜采取的方法是( )
A、Cu
| |||||
B、Cu
| |||||
C、Cu
| |||||
D、Cu
|
下列不属于蛋白质变性的是( )
| A、打针前用酒精消毒 |
| B、蛋白质溶液加入食盐变混浊 |
| C、用稀福尔马林浸泡种子 |
| D、用波尔多液(含硫酸铜)防止作物虫害 |