题目内容
下列反应中,不属于加成反应的是( )
| A、.乙炔与与氯化氢反应制取氯乙烯 |
| B、乙烷和氯气反应制取氯乙烷 |
| C、.乙烯与氢气反应制取乙烷 |
| D、.乙烯通入溴水,溴水褪色 |
考点:取代反应与加成反应
专题:
分析:有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,据此有机物的结构进行判断.
解答:
解:A.乙炔中的三键断裂,两个碳原子上分别结合一个溴原子、氢原子生成氯乙烯,属于加成反应,故A错误;
B.乙烷和氯气反应是乙烷中的H原子被氯原子取代,属于取代反应,故B正确;
C.乙烯中的双键断裂,每个碳原子上结合一个氢原子生成乙烷,属于加成反应,故C错误;
D.乙烯中的双键断裂,每个碳原子上结合一个溴原子生成1,2-二溴乙烯,属于加成反应,故D错误;
故选B.
B.乙烷和氯气反应是乙烷中的H原子被氯原子取代,属于取代反应,故B正确;
C.乙烯中的双键断裂,每个碳原子上结合一个氢原子生成乙烷,属于加成反应,故C错误;
D.乙烯中的双键断裂,每个碳原子上结合一个溴原子生成1,2-二溴乙烯,属于加成反应,故D错误;
故选B.
点评:本题考查有机反应类型,难度不大,注意掌握有机反应类型概念,侧重学生对基础知识的巩固理解.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
能正确表示下列反应的离子方程式为( )
| A、碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH-=CO32-+H2O |
| B、二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O |
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| D、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
下列各组离子在指定环境下能大量共存的是( )
| A、pH=1的溶液中:Na+、S2-、K+、MnO4- |
| B、pH=7的溶液中:Al3+、Cl-、SO42-、HCO3- |
| C、pH>7的溶液中:Na+、AlO2-、SO42-、K+ |
| D、pH=0的溶液中:Na+、K+、Fe2+、ClO- |
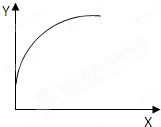 在一恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:2A(g)+B(g)?2C(g);△H<0.当达到平衡后,保持其他条件不变,只改变条件X,则相应量Y的改变一定符合图中曲线的是( )
在一恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:2A(g)+B(g)?2C(g);△H<0.当达到平衡后,保持其他条件不变,只改变条件X,则相应量Y的改变一定符合图中曲线的是( )