题目内容
由K2SO4、Al2(SO4)3 和Na2SO4 组成的混合溶液,c(Na+)=0.1mol/L,c(Al3+)=0.4mol/L,c(SO42-)=0.8mol/L,则 c(K+)为( )
| A、0.15 mol/L |
| B、0.2 mol/L |
| C、0.3 mol/L |
| D、0.4mol/L |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:溶液不显电性,利用电荷守恒:c(K+)+c(Na+)+3c(Al3+)=2c(SO42-)来计算.
解答:
解:设K+的物质的浓度为x,由溶液为电中性可知,c(K+)+c(Na+)+3c(Al3+)=2c(SO42-),则有:
x+0.1mol/L+0.4mol/L×3=0.8mol/L×2,
解得x=0.3mol/L,
故选C.
x+0.1mol/L+0.4mol/L×3=0.8mol/L×2,
解得x=0.3mol/L,
故选C.
点评:本题考查电荷守恒的运用,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
下列各组离子在指定环境下能大量共存的是( )
| A、pH=1的溶液中:Na+、S2-、K+、MnO4- |
| B、pH=7的溶液中:Al3+、Cl-、SO42-、HCO3- |
| C、pH>7的溶液中:Na+、AlO2-、SO42-、K+ |
| D、pH=0的溶液中:Na+、K+、Fe2+、ClO- |
下列电离方程式中,正确的是( )
| A、H2SO4=H2++SO42- |
| B、Ba(OH)2=Ba2++OH- |
| C、NaNO3=Na++NO3- |
| D、MgSO4═Mg+2+SO4-2 |
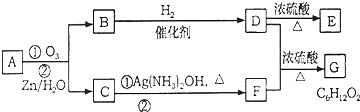
已知苯和一卤代烷在催化剂的作用下可生成苯的同系物: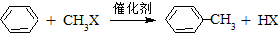 在催化剂的作用下,由苯和下列各组物质合成乙苯,最好应选用的是( )
在催化剂的作用下,由苯和下列各组物质合成乙苯,最好应选用的是( )
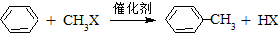 在催化剂的作用下,由苯和下列各组物质合成乙苯,最好应选用的是( )
在催化剂的作用下,由苯和下列各组物质合成乙苯,最好应选用的是( )| A、CH3CH3和Cl |
| B、CH2=CH2和Cl2 |
| C、CH2=CH2和HCl |
| D、CH3CH3和HCl |


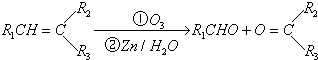
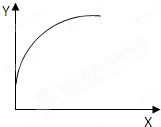 在一恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:2A(g)+B(g)?2C(g);△H<0.当达到平衡后,保持其他条件不变,只改变条件X,则相应量Y的改变一定符合图中曲线的是( )
在一恒容密闭容器中通入A、B两种气体,在一定条件下发生反应:2A(g)+B(g)?2C(g);△H<0.当达到平衡后,保持其他条件不变,只改变条件X,则相应量Y的改变一定符合图中曲线的是( )