题目内容
3.下列各项操作中不发生先沉淀后溶解现象的是( )| A. | 向石灰水中通入过量CO2 | |
| B. | 向Fe(OH)3胶体中逐滴加入过量H2SO4溶液 | |
| C. | 足量NaOH溶液中逐滴加入Al2(SO4)3溶液 | |
| D. | 向NaAlO2溶液中逐滴加入盐酸至过量 |
分析 A.石灰水和CO2反应,生成CaCO3沉淀,继续通入CO2,会与CaCO3反应生成可溶的Ca(HCO3)2;
B.根据胶体的性质判断,加入稀硫酸产生聚沉现象,H2SO4与Fe(OH)3反应;
C.足量NaOH溶液中逐滴加入Al2(SO4)3溶液生成偏铝酸钠;
D.偏铝酸钠和盐酸反应生成氢氧化铝和氯化钠,氢氧化铝和盐酸反应生成氯化铝和水.
解答 解:A.向石灰水中通CO2,反应有:Ca(OH)2+CO2=CaCO3+H2O; CaCO3+H2O+CO2=Ca(HCO3)2,现象为先沉淀后溶解,故A错误;
B.向Fe(OH)3胶体中加入H2SO4会出现先凝聚生成Fe(OH)3沉淀,H2SO4过量,Fe(OH)3与H2SO4反应而溶解,故B错误;
C.足量NaOH溶液中逐滴加入Al2(SO4)3溶液生成偏铝酸钠,不生成沉淀,故C正确;
D.向NaAlO2胶体中逐滴加入过量的稀盐酸,偏铝酸钠先和盐酸反应生成难溶性的氢氧化铝,氢氧化铝是两性氢氧化物能溶于强酸溶液,所以氢氧化铝和盐酸能继续反应生成可溶性的氯化铝,所以出现“先产生沉淀,然后沉淀又溶解”现象,故D错误.
故选C.
点评 本题考查较为综合,涉及元素化合物知识,胶体等,题目难度中等,解答本题的关键是把握物质的性质,注意胶体的性质.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
14.下列过程只涉及化学变化的是( )
| A. | 点石成金 | B. | 酒香不怕巷子深 | C. | 滴水成冰 | D. | 铁棒磨成针 |
18.“保护环境”是我国的基本国策.下列做法不应该提倡的是( )
| A. | 采取低碳、节俭的生活方式 | |
| B. | 按照规定对生活废弃物进行分类放置 | |
| C. | 经常使用一次性筷子、纸杯、塑料袋等 | |
| D. | 改进汽车尾气净化技术,减少大气污染物的排放 |
8.下列离子或分子能够在指定的分散系中大量共存的是( )
| A. | 与铝反应生成大量氢气的溶液中:Mg2+、K+、HCO3-、NO3- | |
| B. | 0.1mol/L的NaNO3溶液中:K+、I-、Cl-、SO42- | |
| C. | 铁与稀硫酸反应后的溶液中:[Fe(CN)6]3-、NH4+、Cl-、NO3- | |
| D. | 空气中:SO2、NO、N2、NH3 |
15.下列化合物能由单质直接化合生成的是( )
| A. | NO2 | B. | FeCl3 | C. | SO3 | D. | FeCl2 |
12.下列化学表达式正确的是( )
| A. | NaHCO3═Na++H++CO32- | B. | Na+2H2O═Na++2OH-+H2↑ | ||
| C. | 2Fe+6H+═Fe3++3H2↑ | D. | NaHSO4═Na++H++SO42- |
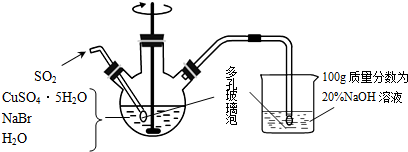
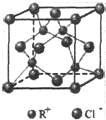 RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.
RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.