题目内容
15.下列化合物能由单质直接化合生成的是( )| A. | NO2 | B. | FeCl3 | C. | SO3 | D. | FeCl2 |
分析 A.氮气与氧气反应生成NO;
B.Fe与氯气反应生成氯化铁;
C.S与氧气反应生成二氧化硫;
D.Fe与氯气反应生成氯化铁.
解答 解:A.氮气与氧气反应生成NO,NO与氧气反应生成二氧化氮,故A不选;
B.Fe与氯气反应生成氯化铁,可由单质直接化合生成,故B选;
C.S与氧气反应生成二氧化硫,二氧化硫催化氧化生成三氧化硫,故C不选;
D.Fe与氯气反应生成氯化铁,不能生成氯化亚铁,故D不选;
故选B.
点评 本题考查金属的性质,为高频考点,把握发生的氧化还原反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列叙述正确的是( )
| A. | 棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O | |
| B. | 清洁能源所用光电池的生产材料主要是用高纯度的二氧化硅 | |
| C. | 在医疗上氢氧化铝可用于治疗胃酸过多 | |
| D. | 漂白粉在使用时一定要加入一定量的盐酸才能起到漂白作用 |
3.下列各项操作中不发生先沉淀后溶解现象的是( )
| A. | 向石灰水中通入过量CO2 | |
| B. | 向Fe(OH)3胶体中逐滴加入过量H2SO4溶液 | |
| C. | 足量NaOH溶液中逐滴加入Al2(SO4)3溶液 | |
| D. | 向NaAlO2溶液中逐滴加入盐酸至过量 |
10.关于Na2CO3和NaHCO3性质的说法正确的是( )
| A. | 等浓度时水溶液碱性:NaHCO3>Na2CO3 | |
| B. | 热稳定性:NaHCO3>Na2CO3 | |
| C. | 与盐酸溶液反应的速率(快慢):NaHCO3<Na2CO3 | |
| D. | 等质量的Na2CO3、NaHCO3分别与足量的盐酸反应,NaHCO3产生的CO2多 |
20. 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
(1)COCl2的空间构型为平面三角形;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式分解. A.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsCl+ICl B.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsI+Cl2
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘.
(4)下列分子既不存在s-p σ键,也不存在p-p π键的是D.
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中中心氯原子的杂化轨道类型为sp3杂化,写出与CN-互为等电子体的分子:N2或 CO(写出1个).
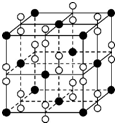
(6)钙在氧气中燃烧时得到一种钙的氧化物固体,其结构如图所示.由此可判断该钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g•cm-3,则晶胞中离得最近的两个钙离子间的距离为$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$ cm(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA).
 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.(1)COCl2的空间构型为平面三角形;溴的价电子排布式为4s24p5.
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列A式分解. A.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsCl+ICl B.CsICl2$\frac{\underline{\;\;△\;\;}}{\;}$CsI+Cl2
(3)根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘.
| 氟 | 氧 | 溴 | 碘 | |
| 第一电离能 (kJ/mol) | 1 681 | 1 251 | 1 140 | 1 008 |
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为角型,中心氯原子周围有四对价层电子.ClO2-中中心氯原子的杂化轨道类型为sp3杂化,写出与CN-互为等电子体的分子:N2或 CO(写出1个).
(6)钙在氧气中燃烧时得到一种钙的氧化物固体,其结构如图所示.由此可判断该钙的氧化物的化学式为CaO2.已知该氧化物的密度是ρ g•cm-3,则晶胞中离得最近的两个钙离子间的距离为$\frac{\sqrt{2}}{2}$×$\root{3}{\frac{72×4}{ρN{\;}_{A}}}$ cm(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA).
5.向FeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤沉淀,然后在空气中灼烧沉淀,最终得到的固体物质是( )
| A. | Fe2O3 | B. | FeO | C. | Fe(OH)3 | D. | Fe3O4 |