题目内容
17.下列描述的一定是金属元索的是( )| A. | 原子核内有4个质子的元素 | B. | 能与水反应的单质 | ||
| C. | 原子的最外层只有2个电子的元素 | D. | 能形成离子化合物的元素 |
分析 A.原子核内有4个质子的元素为Be;
B.活泼金属单质以及部分非金属单质都可与水反应;
C.原子的最外层只有2个电子的元素可能为He;
D.能形成离子化合物的元素可全部为非金属性元素.
解答 解:A.原子核内有4个质子的元素为Be,为金属元素,故A正确;
B.活泼金属单质以及部分非金属单质都可与水反应,如氯气、氟气等都可与水反应,但为非金属,故B错误;
C.原子的最外层只有2个电子的元素可能为He,为非金属,故C错误;
D.能形成离子化合物的元素可全部为非金属性元素,如铵盐,故D错误.
故选A.
点评 本题主要考查度元素的性质等考点的理解,为高频考点,侧重于学生的分析能力的考查,难度不大,B选项为易错点,注意利用反例法进行的解答.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
12.某溶液中含如下离子组中的若干种:K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-,某同学欲探究该溶液的组成,进行如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色,下列说法正确的是( )
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色,下列说法正确的是( )
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 步骤Ⅱ中无色气体是NO气体,无CO2气体产生 | |
| C. | 原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- | |
| D. | 为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
2.下列钢铁腐蚀属于原电池原理的是( )
| A. | 吸氧腐蚀 | B. | 与稀盐酸反应 | ||
| C. | 与氧气反应 | D. | 高温下与水蒸气反应 |
7.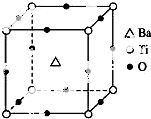 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )| A. | 8 BaTi8O12 | B. | 8 BaTi4O9 | C. | 6 BaTiO3 | D. | 3 BaTi2O3 |
4.下列化学用语表示正确的是( )
| A. | 钾离子结构示意图: | |
| B. | N2H4的电子式: | |
| C. | 聚丙烯的结构简式: | |
| D. | 中子数为79、质子数为55的铯(Cs)原子:${\;}_{55}^{79}$Cs |
5.某小组用如图装置进行实验,下列说法正确的是( )
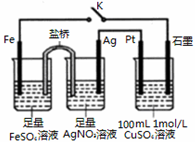

| A. | 盐桥中的电解质可以用KC1 | |
| B. | 闭合K,石墨电极上只生成铜 | |
| C. | 当有0.1mol Fe溶解时,流经电解液的电子个数为1.204×1023 | |
| D. | 导线中流过0.3mol电子时,加入11.1gCu2(OH)2CO3,CuSO4溶液可恢复原组成 |
 ,从共用电子对是否偏移的角度,说明在H2O2中的共价键的不同之处:H、O之间极性共价键,O、O之间非极性共价键.
,从共用电子对是否偏移的角度,说明在H2O2中的共价键的不同之处:H、O之间极性共价键,O、O之间非极性共价键.