题目内容
12.某溶液中含如下离子组中的若干种:K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-,某同学欲探究该溶液的组成,进行如下实验:Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色,下列说法正确的是( )
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 步骤Ⅱ中无色气体是NO气体,无CO2气体产生 | |
| C. | 原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- | |
| D. | 为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
分析 Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰,证明含有K+;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,即为二氧化氮,此时溶液颜色加深,但无沉淀生成,说明含有NO3-以及还原性的离子,且不含有SiO32-;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,即为硫酸钡,再滴加KSCN溶液,上层清液变红,含有Fe3+离子,第二支试管中加入CCl4,充分振荡静置后溶液分层,下层出现紫红色,证明有碘单质生成,则含有K+、Fe2+、NO3-、SO42-、I-,以此解答该题.
解答 解:Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰,证明含有K+;
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,即为二氧化氮,此时溶液颜色加深,但无沉淀生成,说明含有NO3-以及还原性的离子,且不含有SiO32-;
Ⅲ.取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,即为硫酸钡,再滴加KSCN溶液,上层清液变红,含有Fe3+离子,第二支试管中加入CCl4,充分振荡静置后溶液分层,下层出现紫红色,证明有碘单质生成,则含有K+、Fe2+、NO3-、SO42-、I-,
A.由以上分析可知含有Fe2+、NO3-、SO42-、I-等离子,故A错误;
B.由以上分析可知生成气体为NO,因含有Fe2+,则不存在CO32-,生成气体中不含二氧化碳,故B正确;
C.因含有I-,则不存在氧化性的Fe3+,故C错误;
D.因含有SO42-,加入硝酸银可生成硫酸银沉淀,干扰实验结论,故D错误;
故选B.
点评 本题考查无机物的推断,着重考查物质的检验、鉴别,为高频考点,侧重于学生的分析能力的考查,题目难度中等,解答本题的关键是把握发生的有关化学反应确定存在的离子.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 制取氧气时,用排水法收集氧气出现倒吸现象,立即打开试管上的橡皮塞 | |
| B. | 在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度 | |
| C. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| D. | 给试管中的液体加热时,不停沿试管倾斜方向移动试管或加入碎瓷片,以免液体暴沸伤人 |
| A. | 1.8 g 重水(D2O)中含有的中子数为NA | |
| B. | 常温常压下,22.4 L O2 含有的分子数为NA | |
| C. | 1 L 1 mol/L FeCl3溶液中含有Fe3+的数目为NA | |
| D. | 0.1 mol CO2分子中含有的共用电子对的数目是0.4 NA |
| A. | 容器内压强不随时间变化 | |
| B. | v正(X)=v逆(Z) | |
| C. | 容器内X、Y、Z的浓度之比为l:2:2 | |
| D. | 单位时间内消耗0.1 mol X的同时生成0.2 mol Z |
| A. | 原子核内有4个质子的元素 | B. | 能与水反应的单质 | ||
| C. | 原子的最外层只有2个电子的元素 | D. | 能形成离子化合物的元素 |
| A. | 原子核外电子排布式为1s2的原子与原子核外电子排布式为1s22s2的原子化学性质相似 | |
| B. | Zn2+核外电子排布式为1s22s22p63s23p63d10 | |
| C. | 基态铜原子的外围电子排布图: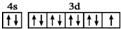 | |
| D. | 基态碳原子的最外层电子排布图: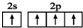 |
| A. | HF、HCl、HBr、HI热稳定性依次减弱 | |
| B. | NaF、NaCl、NaBr、NaI的熔点依次降低 | |
| C. | 金刚石的硬度大于硅,其熔、沸点也高于硅 | |
| D. | F2、Cl2、Br2、I2的熔、沸点逐渐升高 |