题目内容
5.(1)将6g CH3COOH溶于水制成1L溶液,此溶液的物质的量浓度为0.1mol/L,经测定溶液中含CH3COO-为1.4×10-3mol/L,此温度下醋酸的电离度=1.4%,温度升高,Ka将变大.(2)25℃时,pH=12.0的KOH溶液中,由水电离出的C(OH-)=10-12mol/L.
(3)常温下,将0.1mol•L-1氢氧化钠溶液与0.06mol•L-1硫酸溶液等体积混合,该混合溶液的pH等于2.
分析 (1)n(CH3COOH)=$\frac{6g}{60g/mol}$=0.1mol,根据c=$\frac{n}{V}$计算物质的量浓度;根据α=$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$计算电离度,结合外界条件对弱电解质的电离平衡的影响判断电离度的变化;
(2)碱抑制水电离,碱溶液中水电离出的氢氧根离子浓度等于溶液中氢离子浓度;
(3)根据酸碱溶液混合时,先判断过量,然后计算过量的酸或碱的物质的量浓度,最后计算溶液的pH来解答即可.
解答 解:(1)n(CH3COOH)=$\frac{6g}{60g/mol}$=0.1mol,
c(CH3COOH)=$\frac{0.1mol}{1L}$=0.1mol/L,
α=$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=$\frac{1.4×1{0}^{-3}}{0.1}$=1.4%,弱电解质电离吸热,故升高温度,醋酸的电离平衡右移,即Ka变大.
故答案为:0.1mol/L;1.4%;变大;
(2)碱抑制水电离,碱溶液中水电离出的c(OH-)=c(H+)=10-12 mol/L,故答案为:10-12;
(3)设溶液的体积都是1L,则氢氧化钠的物质的量为1L×0.1mol•L-1=0.1mol,
硫酸的物质的量为1L×0.06mol•L-1=0.06mol,H+的物质的量为0.06mol×2=0.12mol,
则当酸碱发生中和时H+和OH-的物质的量分别为0.12mol和0.1mol,
则硫酸过量,过量的H+的物质的量为0.12mol-0.1mol=0.02mol,
则反应后溶液中H+的物质的量浓度为c(H+)=$\frac{0.02mol}{2L}$=0.01 mol•L-1,
pH=-lg10-2=2.
故答案为:2.
点评 本题主要考查溶液pH的有关计算和溶液中水电离出氮气氢离子、氢氧根的浓度的计算,明确酸碱反应的过量分析是解答的关键,并应熟悉物质的量的计算、pH的计算公式来解答即可.

 阅读快车系列答案
阅读快车系列答案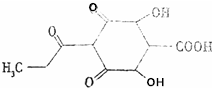 一种植物生长调节的结构简式如图所示,下列说法不正确的是( )
一种植物生长调节的结构简式如图所示,下列说法不正确的是( )| A. | 该物质含有3种官能团 | B. | 该物质属于脂环烃 | ||
| C. | 该物质属于多官能团化合物 | D. | 该物质属于烃的衍生物 |
| A. | 1.8 g 重水(D2O)中含有的中子数为NA | |
| B. | 常温常压下,22.4 L O2 含有的分子数为NA | |
| C. | 1 L 1 mol/L FeCl3溶液中含有Fe3+的数目为NA | |
| D. | 0.1 mol CO2分子中含有的共用电子对的数目是0.4 NA |
| A. | 物质的量浓度相同的盐酸和CH3COOH溶液 | |
| B. | 物质的量浓度相同的NaOH溶液和氨水 | |
| C. | pH=3的盐酸和pH=3的NH4Cl溶液均稀释100倍所得溶液 | |
| D. | pH=10的NaOH溶液和pH=10的CH3COONa溶液均稀释100倍所得溶液 |
| A. | 原子核内有4个质子的元素 | B. | 能与水反应的单质 | ||
| C. | 原子的最外层只有2个电子的元素 | D. | 能形成离子化合物的元素 |
| A. | c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)>c(OH-) | |
| C. | c(CH3 COO-)=c(Cl-)>c(H+)>c(CH3COOH)>c(OH-) | |
| D. | c(Cl-)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| A. | 铜与稀硝酸反应制取NO2 | |
| B. | 碳酸钙与稀盐酸反应制取二氧化碳 | |
| C. | 双氧水在MnO2催化下反应制取氧气 | |
| D. | 氯化铵固体与氢氧化钙固体混合加热制取氨气 |