题目内容
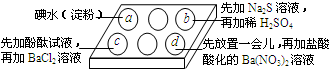 为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3 溶液,再分别滴加用如图所示的试剂对实验现象的“解释或结论”错误的是( )
为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3 溶液,再分别滴加用如图所示的试剂对实验现象的“解释或结论”错误的是( )| 选项 | 实验现象 | 解释或结论 |
| A | a中溶液褪色 | 还原性:SO32-<I- |
| B | b中加硫酸后产生淡黄色沉淀 | SO32-和S2-在酸性条件下发生反应 |
| C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪去 | SO32-+H2O?HSO3-+OH-,所以滴入酚酞变红; Ba2++SO32-→BaSO3↓(白),使水解平衡左移,红色褪去 |
| D | d中产生白色沉淀 | Na2SO3溶液已被氧化变质 |
| A、A | B、B | C、C | D、D |
考点:含硫物质的性质及综合应用
专题:氧族元素
分析:A、Na2SO3溶液中亚硫酸钠具有还原性和碘单质反应生成硫酸钠;
B、Na2SO3溶液与硫化钠、硫酸溶液发生氧化还原反应生成淡黄色硫单质沉淀;
C、Na2SO3溶液水解显碱性,使酚酞变红,加入氯化钡会结合亚硫酸根离子形成亚硫酸钡沉淀,水解平衡逆向进行,氢氧根离子浓度减小红色褪去;
D、亚硫酸钠具有还原性,能被硝酸氧化为硫酸钠,硫酸钠可以和氯化钡反应生成硫酸钡沉淀,该沉淀不溶于盐酸.
B、Na2SO3溶液与硫化钠、硫酸溶液发生氧化还原反应生成淡黄色硫单质沉淀;
C、Na2SO3溶液水解显碱性,使酚酞变红,加入氯化钡会结合亚硫酸根离子形成亚硫酸钡沉淀,水解平衡逆向进行,氢氧根离子浓度减小红色褪去;
D、亚硫酸钠具有还原性,能被硝酸氧化为硫酸钠,硫酸钠可以和氯化钡反应生成硫酸钡沉淀,该沉淀不溶于盐酸.
解答:
解:A、Na2SO3溶液中亚硫酸钠具有还原性,可以和碘单质反应生成硫酸钠、碘化钠,亚硫酸钠做还原剂,碘化钠是还原产物,所以还原性:SO32->I-,故A错误;
B、Na2SO3溶液中硫元素是+4价,硫化钠中硫元素是-2价,二者可以和硫酸溶液发生氧化还原反应,硫元素归中到0价,即生成淡黄色硫单质沉淀,故B正确;
C、Na2SO3溶液亚硫酸根离子水解显碱性,该溶液会使酚酞变红,加入氯化钡会结合亚硫酸根离子形成亚硫酸钡沉淀,水解平衡逆向进行,氢氧根离子浓度减小,碱性逐渐消失,所以红色褪去,故C正确;
D、亚硫酸钠具有还原性,加入盐酸酸化的硝酸钡,即相当于加入了硝酸,亚硫酸根离子能被硝酸氧化为硫酸根,硫酸根离子可以和钡离子反应生成硫酸钡沉淀,该沉淀不溶于硝酸,所以实验证明的是亚硫酸根离子的还原性,是被硝酸氧化的缘故,故D错误.
故选AD.
B、Na2SO3溶液中硫元素是+4价,硫化钠中硫元素是-2价,二者可以和硫酸溶液发生氧化还原反应,硫元素归中到0价,即生成淡黄色硫单质沉淀,故B正确;
C、Na2SO3溶液亚硫酸根离子水解显碱性,该溶液会使酚酞变红,加入氯化钡会结合亚硫酸根离子形成亚硫酸钡沉淀,水解平衡逆向进行,氢氧根离子浓度减小,碱性逐渐消失,所以红色褪去,故C正确;
D、亚硫酸钠具有还原性,加入盐酸酸化的硝酸钡,即相当于加入了硝酸,亚硫酸根离子能被硝酸氧化为硫酸根,硫酸根离子可以和钡离子反应生成硫酸钡沉淀,该沉淀不溶于硝酸,所以实验证明的是亚硫酸根离子的还原性,是被硝酸氧化的缘故,故D错误.
故选AD.
点评:本题考查学生含硫元素的化合物的性质,注意亚硫酸根离子、硫离子的强还原性,综合性强,难度不大.

练习册系列答案
相关题目
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,2克氢气所含原子数目为NA |
| B、4.6克钠与水反应时失去的电子数目为0.2NA |
| C、在标准状况下,22.4LNH3所含的质子数目为NA |
| D、1 L0.5mol?L-1Na2SO4溶液中所含有的Na+离子数目为2NA |
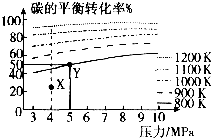 已知给煤炭加氢可发生反应:C(s)+2H2(g)?CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( )
已知给煤炭加氢可发生反应:C(s)+2H2(g)?CH4(g).在VL的容器中投入amol碳(足量),同时通入2amolH2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示.下列说法正确的是( )| A、上述正反应为放热反应 | ||
| B、在4MPa、1200K时,图中X点v(H2)正>v(H2)逆 | ||
C、在5MPa、800K时,该反应的平衡常数为
| ||
| D、工业上维持6MPa1000K而不采用10MPa1000K,主要是因为前者碳的转化率高 |
下列有关说法正确的是( )
| A、钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生 |
| B、反应NH4Cl(s)=NH3(g)+HCl(g)在室温下不能自发进行,则该反应的△H>0 |
| C、由于Ksp(BaSO4)<Ksp(BaCO3),因此BaSO4沉淀不可能转化为BaCO3沉淀 |
| D、25℃时,0.1 mol?L-1CH3COOH溶液加水稀释后,c(OH-)/c(CH3COOH)增大 |
将0.2mol/L的FeBr2与0.1mol/L FeI2溶液等体积混合后,慢慢通入一定体积的氯气,可能发生的离子反应方程式为( )
| A、Cl2+2Fe2+→2Cl-+2Fe3+ |
| B、2Cl2+2Fe2++2I-=2Fe3++4Cl-+I2 |
| C、3Cl2+2Fe2++4Br-→2Fe3++6Cl-+2Br2 |
| D、6Cl2+6Fe2++4I-+2Br-=6Fe3++12Cl-+2I2+Br2 |
下列对非金属元素(除稀有气体元素外)的相关判断正确的是( )
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价.
①非金属元素都是主族元素
②单质在反应中都只能作氧化剂
③氢化物常温下都是气态,所以都叫气态氢化物
④氧化物常温下都可以与水反应生成酸
⑤非金属元素R所形成的含氧酸盐(MaROb)中的R元素必定呈现正价.
| A、②⑤ | B、①③⑤ |
| C、②③④ | D、①⑤ |
以下说法正确的是( )
| A、少量的金属钠长期暴露在空气中,它的最终产物是NaHCO3 |
| B、向紫色石蕊溶液中加入过量Na2O2粉末,振荡,产生气泡,溶液仍为紫色 |
| C、CO与H2混合气体3 g和足量的氧气燃烧后,在150℃时将混合气体通过足量的Na2O2后,Na2O2增重的质量为3g |
| D、将1g Na2CO3和NaHCO3分别溶于10mL水中,滴入酚酞试液后溶液所显红色深浅相同 |