题目内容
6.用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(CN-)<c(Na+),下列关系式正确的是( )| A. | c(H+)<c(OH-) | B. | c(HCN)<c(CN-) | ||
| C. | c(CN-)+c(OH-)=0.1mol?L-1 | D. | c(HCN)+c(CN-)=0.2mol?L-1 |
分析 物质的量都是0.1mol的HCN和NaCN配成1L混合溶液,已知其中c(CN-)小于c(Na+),根据溶液电中性原则,溶液中存在电荷守恒c(CN-)+c(OH-)=c(Na+)+c(H+),则存在c(H+)<c(OH-),溶液应呈碱性,结合电荷守恒、物料守恒等知识解答该题.
解答 解:A.物质的量都是0.1mol的HCN和NaCN配成1L混合溶液,已知其中c(CN-)小于c(Na+),根据溶液电中性原则,溶液中存在电荷守恒c(CN-)+c(OH-)=c(Na+)+c(H+),则存在c(H+)<c(OH-),溶液应呈碱性,故A正确;
B.混合溶液呈碱性,说明酸的电离程度小于酸根离子水解程度,则c(HCN)>c(CN-),故B错误;
C.溶液中存在c(CN-)+c(OH-)=c(Na+)+c(H+),因c(Na+)=0.1mol/L,则c(CN-)+c(OH-)>0.1mol/L,故C错误;
D.HCN和NaCN的物质的量都为1mol,由物料守恒可知c(CN-)+c(HCN)=0.2mol/L,故D正确;
故选AD.
点评 本题考查离子浓度大小比较,题目难度中等,明确溶液酸碱性是解本题关键,注意把握离子浓度大小的比较方法,解题时注意守恒思想的应用.

练习册系列答案
相关题目
17.下列物质中,属于单质的是 ( )
| A. | HCl | B. | CO2 | C. | Br2 | D. | NaOH |
14.设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,22.4 L CCl4含有4nA个Cl原子 | |
| B. | 常温常压下,18 g H2O中含有2nA个氢原子 | |
| C. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| D. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标况下,44.8 L的水中含有H2O分子的数目为2 NA | |
| B. | 常温常压下,22.4 L氢气中含氢原子数目为2 NA | |
| C. | 物质的量浓度为0.5 mol/L的NaCl溶液中,含有Cl-个数为0.5 NA | |
| D. | 5.6 g Fe在足量氯气中完全反应,失去的电子数为0.3 NA |
11.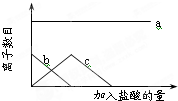 向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化.坐标系中a、b、c三条曲线分别对应的离子是( )
向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化.坐标系中a、b、c三条曲线分别对应的离子是( )
 向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化.坐标系中a、b、c三条曲线分别对应的离子是( )
向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化.坐标系中a、b、c三条曲线分别对应的离子是( )| A. | Na+ CO32- H+ | B. | Cl-Na+ CO32- | ||
| C. | Na+HCO3- CO32- | D. | Na+ CO32- HCO3- |
18.下列有关说法正确的是( )
| A. | 加水稀释,盐溶液中各离子的物质的量浓度均将减小 | |
| B. | 常温下反应4Fe(OH)2+O2+2H2O═4Fe(OH)3能自发进行,则△H<0 | |
| C. | 足量的锌与等体积等pH的HA、HB溶液分别反应,HA放出的氢气少说明是强酸 | |
| D. | 葡萄糖中花青素在碱性环境下显紫色,故可用苏打粉检验假红酒 |
16.下列有关说法正确的是( )
| A. | HClO是弱酸,但它的氧化能力很强 | |
| B. | S在纯净的氧气中易被氧化为SO3 | |
| C. | 在氯酸钾溶液中含有少量自由移动的氯离子 | |
| D. | 22.4LCl2(标准状况),在反应中总是转移2NA个电子 |
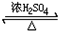 CH3COOC2H5+H2O、酯化反应(取代反应).
CH3COOC2H5+H2O、酯化反应(取代反应).