题目内容
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 标况下,44.8 L的水中含有H2O分子的数目为2 NA | |
| B. | 常温常压下,22.4 L氢气中含氢原子数目为2 NA | |
| C. | 物质的量浓度为0.5 mol/L的NaCl溶液中,含有Cl-个数为0.5 NA | |
| D. | 5.6 g Fe在足量氯气中完全反应,失去的电子数为0.3 NA |
分析 A.标况下,水为液态;
B.气体摩尔体积的应用条件是标准状况;
C.溶液的体积未知,无法计算;
D.铁和氯气反应生成氯化铁.
解答 解:A.标况下,水为液态,不能根据气体摩尔体积来计算,故A错误;
B.气体摩尔体积的应用条件是标准状况,温度压强不知,22.4L氢气中物质的量不是1mol,故B错误;
C.该题中溶液的体积未知,无法计算氯离子的个数,故C错误;
D.5.6g铁粉物质的量为0.1mol,与氯气反应生成氯化铁,失去的电子数为0.3NA,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是物质的量和微粒数的计算应用,气体摩尔体积的条件应用分析,题目较简单.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
11.下列有关金属腐蚀与防护的说法正确的是( )
| A. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| B. | 可将地下输油钢管与外加直流电的正极相连以保护它不受腐蚀 | |
| C. | 自然界中钢铁的腐蚀以析氢腐蚀为主 | |
| D. | 生铁在海水中的腐蚀速度比在空气中快 |
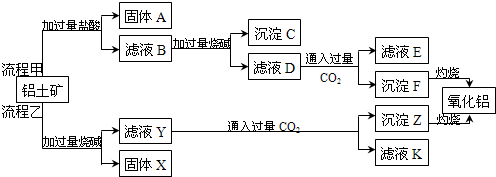
9.(一)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)中提取氧化铝的两种工艺流程如下:
已知:
生成氢氧化物沉淀的pH
请回答下列问题
(1)固体A的主要化学成分是:SiO2(填化学式),
(2)流程乙加入烧碱后生成AlO2-的离子方程式为:Al2O3+2OH-=2AlO2-+H2O
(3)验证滤液B中含有Fe3+的实验操作为:取少量滤液B于试管中,滴加1-2滴硫氰化钾溶液,若溶液变为血红色,则说明滤液B中含有Fe3+
(4)不管是流程甲还是流程乙,都会对铝土矿进行粉碎,原因是:增大固液接触面积,加快反应速率
(5)滤液B也可以通过控制溶液的pH加入氢氧化钠直接得到沉淀F,应调节pH范围为3.2≤pH<3.4.
(二)有机化学
(6)新戊烷的系统命名法命名为:2,3-二甲基丙烷.
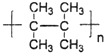
(7)按照官能团的分类,有机物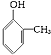 的类别是:酚.
的类别是:酚.
(8)乙酸的核磁共振氢谱图有2个吸收峰,面积比为:1:3或3:1.

已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
(1)固体A的主要化学成分是:SiO2(填化学式),
(2)流程乙加入烧碱后生成AlO2-的离子方程式为:Al2O3+2OH-=2AlO2-+H2O
(3)验证滤液B中含有Fe3+的实验操作为:取少量滤液B于试管中,滴加1-2滴硫氰化钾溶液,若溶液变为血红色,则说明滤液B中含有Fe3+
(4)不管是流程甲还是流程乙,都会对铝土矿进行粉碎,原因是:增大固液接触面积,加快反应速率
(5)滤液B也可以通过控制溶液的pH加入氢氧化钠直接得到沉淀F,应调节pH范围为3.2≤pH<3.4.
(二)有机化学
(6)新戊烷的系统命名法命名为:2,3-二甲基丙烷.
(7)按照官能团的分类,有机物
 的类别是:酚.
的类别是:酚.(8)乙酸的核磁共振氢谱图有2个吸收峰,面积比为:1:3或3:1.
16.下列反应的离子方程式,正确的是( )
| A. | Fe溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+ | |
| D. | 铝与浓氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
6.用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(CN-)<c(Na+),下列关系式正确的是( )
| A. | c(H+)<c(OH-) | B. | c(HCN)<c(CN-) | ||
| C. | c(CN-)+c(OH-)=0.1mol?L-1 | D. | c(HCN)+c(CN-)=0.2mol?L-1 |
11.下列反应中的氨与反应4NH3+5O2═4NO+6H2O中的氨作用相同的是( )
| A. | NaOH+NH4Cl═NaCl+NH3↑+H2O | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | 2Na+2NH3═2NaNH2+H2↑ | D. | NH3+CO2+H2O═NH4HCO3 |
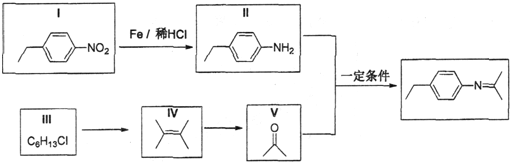

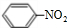 ,Z的结构简式为
,Z的结构简式为