题目内容
11.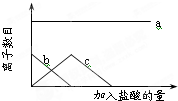 向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化.坐标系中a、b、c三条曲线分别对应的离子是( )
向一定量的Na2CO3溶液中缓慢滴入稀盐酸,并不断搅拌,随着盐酸的加入,溶液中自由离子的数目也随之发生如图所示变化.坐标系中a、b、c三条曲线分别对应的离子是( )| A. | Na+ CO32- H+ | B. | Cl-Na+ CO32- | ||
| C. | Na+HCO3- CO32- | D. | Na+ CO32- HCO3- |
分析 根据向一定量的Na2CO3溶液中缓慢地滴加稀盐酸,则先后发生Na2CO3+HCl═NaCl+NaHCO3、NaHCO3+HCl═NaCl+CO2↑+H2O,则钠离子数目不发生变化,氯离子的数目在增加,碳酸根离子的数目一直在减少,直到为0,碳酸氢根离子的数目先增大后减小,直到为0,然后结合图象来分析对应的离子.
解答 解:向一定量的Na2CO3溶液中缓慢地滴加稀盐酸,则先后发生Na2CO3+HCl═NaCl+NaHCO3、NaHCO3+HCl═NaCl+CO2↑+H2O,
钠离子数目不变,则即图中a为Na+离子,
酸根离子在减少,直至为0,即图中b为CO32-离子,
碳酸氢根离子先增大后减小,直至为0,即图中c为HCO3-离子,
故选D.
点评 本题以碳酸钠与盐酸的反应来分析溶液中离子的变化,题目难度中等,侧重于学生的分析能力的考查,明确离子反应的实质并学会结合图象来判断离子数目是解答的关键.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
2.在溶液中能大量共存的离子组是( )
| A. | K+、Fe3+、SCN-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Cl-、CO32- | D. | Na+、Cu2+、Cl-、SO42- |
19.化学知识可以帮助理解和解决日常生活中遇到的许多问题,下列说法错误的是( )
| A. | 胃酸过多的病人,可以服用氢氧化钠来中和胃酸 | |
| B. | 晶体硅是在通信工程中制作光导纤维的主要原料 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存 | |
| D. | 二氧化硅与氢氟酸的反应原理可用来雕刻玻璃 |
6.用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(CN-)<c(Na+),下列关系式正确的是( )
| A. | c(H+)<c(OH-) | B. | c(HCN)<c(CN-) | ||
| C. | c(CN-)+c(OH-)=0.1mol?L-1 | D. | c(HCN)+c(CN-)=0.2mol?L-1 |
16.下列化合物的核磁共振氢谱中出现三组峰的是( )
| A. | 甲苯 | B. | 1,3-丁二烯 | C. | 2-甲基丙烷 | D. | 2,4-二甲基戊烷 |
3.二氧化硫能够使高锰酸钾溶液褪色,表现了二氧化硫的( )
| A. | 酸性 | B. | 氧化性 | C. | 还原性 | D. | 漂白性 |
20.在高炉中,还原氧化铁的物质是( )
| A. | 二氧化碳 | B. | 铁矿石 | C. | 石灰石 | D. | 一氧化碳 |
1.下列实验操作正确的是( )
| A. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| B. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,则该溶液一定是碳酸盐溶液 | |
| C. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| D. | 中和热测定实验中,要将酸和碱迅速混合,以防热量散失 |