题目内容
13.以下化学反应关系转化图中,A的焰色反应呈黄色,E、F为有刺激性气味的气体,F也是造成酸雨的主要成分,G为强酸性溶液,H为既难溶于水、也难溶于稀酸的白色固体.试回答: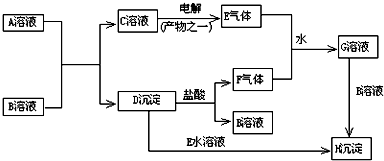
(1)写出化学式:ANa2SO3;BBaCl2.
(2)写出下列反应的化学方程式或离子方程式:
①C→E(化学方程式):2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑
②D+E+H2O→H(化学方程式):BaSO3+Cl2+H2O=BaSO4↓+2HCl
③E+F+H2O→G(离子方程式):SO2+Cl2+2H2O=SO42-+4H++2Cl-
(3)C溶液电解的另一气体产物的燃烧热为285.8kJ/mol,写出该物质燃烧的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O (l)△H=-285.8kJ/mol.
(4)将F气体通入品红溶液中的现象是品红溶液褪色,由此现象说明F气体具有的性质是漂白性.
分析 A的焰色反应呈黄色,则A中含有钠元素,E、F为有刺激性气味的气体,电解C的溶液得到气体E,沉淀D与盐酸反应得到气体F,E、F和水反应生成G,G为强酸性溶液,则E、F为二氧化硫和氯气,F也是造成酸雨的主要成分,则E为Cl2,F为SO2,G中含有HCl、H2SO4,D与E的溶液生成H沉淀,H为既难溶于水、也难溶于稀酸的白色固体,则H为BaSO4,D为BaSO3,B为BaCl2,A为Na2SO3,C为NaCl.
解答 解:A的焰色反应呈黄色,则A中含有钠元素,E、F为有刺激性气味的气体,电解C的溶液得到气体E,沉淀D与盐酸反应得到气体F,E、F和水反应生成G,G为强酸性溶液,则E、F为二氧化硫和氯气,F也是造成酸雨的主要成分,则E为Cl2,F为SO2,G中含有HCl、H2SO4,D与E的溶液生成H沉淀,H为既难溶于水、也难溶于稀酸的白色固体,则H为BaSO4,D为BaSO3,B为BaCl2,A为Na2SO3,C为NaCl.
(1)由上述分析可知,A为Na2SO3,B为BaCl2,
故答案为:Na2SO3;BaCl2;
(2)①反应C→E的化学方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑,
②D+E+H2O→H的化学方程式):BaSO3+Cl2+H2O=BaSO4↓+2HCl,
③E+F+H2O→G的离子方程式为:SO2+Cl2+2H2O=SO42-+4H++2Cl-,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑;BaSO3+Cl2+H2O=BaSO4↓+2HCl;SO2+Cl2+2H2O=SO42-+4H++2Cl-;
(3)电解氯化钠溶液得到氯气以外的气体为氢气,氢气燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O (l)△H=-285.8kJ/mol,
故答案为:H2(g)+$\frac{1}{2}$O2(g)=H2O (l)△H=-285.8kJ/mol;
(4)F为SO2,将F气体通入品红溶液中的现象是:品红溶液褪色,由此现象说明F气体具有的性质是漂白性,
故答案为:品红溶液褪色;漂白性.
点评 本题考查无机物的推断,A的焰色反应呈黄色,E、F为有刺激性气味的气体,G为强酸性溶液等是推断突破口,再结合转化关系进行推断,对学生的逻辑推理能力提出较高的要求,很好地考查学生的思维、推断、分析能力,熟练掌握元素化合物性质,题目难度中等.

 考前必练系列答案
考前必练系列答案| A. | 78 g Na2O2中存在的共价键总数为NA | |
| B. | 0.1 mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 氢氧燃料电池负极消耗2.24 L气体时,电路中转移的电子数为0.1NA | |
| D. | 0.1 mol氯化铁溶于1L水中,所得溶液中Fe3+的数目为0.1NA |
| A. | 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g | |
| B. | 1 molNa2O2固体中含离子总数为4NA | |
| C. | 1mol羟基与17gNH3所含电子数之比为9:10 | |
| D. | 1molNa2CO3晶体中含CO32-离子数小于NA |
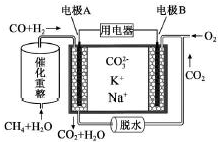
| A. | 正极产物为CO2 | |
| B. | 负极电极反应式为CO-2e-+CO32-═2CO2 | |
| C. | 电池工作时,CO32-向电极A移动 | |
| D. | 电池总反应式为CO+H2+O2═2CO2+H2O |
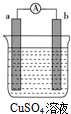 某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题:
某原电池的装置如图所示,看到a极上有红色金属析出,回答下列问题: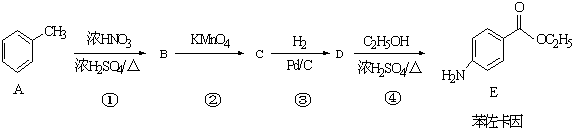
 .
.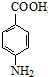 +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$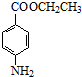 +H2O
+H2O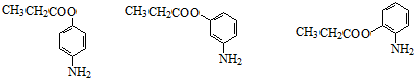 (其中一种)(任写一种)
(其中一种)(任写一种) )的合成路线图(其他原料任选).
)的合成路线图(其他原料任选).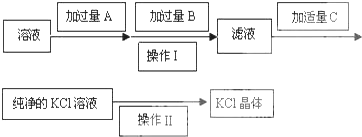
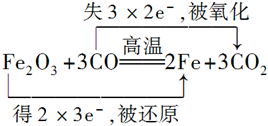 .
.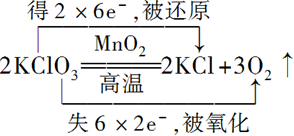 .
. .
.