题目内容
20.设NA为阿伏加德罗常数,下列叙述中正确的是( )| A. | 78 g Na2O2中存在的共价键总数为NA | |
| B. | 0.1 mol${\;}_{38}^{90}$Sr原子中含中子数为3.8NA | |
| C. | 氢氧燃料电池负极消耗2.24 L气体时,电路中转移的电子数为0.1NA | |
| D. | 0.1 mol氯化铁溶于1L水中,所得溶液中Fe3+的数目为0.1NA |
分析 A.1molNa2O2中存在1mol共价键;
B.元素符号的左下角为质子数;
C.气体不一定在标况下;
D.氯化铁溶液中铁离子部分水解,导致铁离子数目减少.
解答 解:A.78 g Na2O2的物质的量为1mol,存在的共价键总数为NA,故A正确;
B.${\;}_{38}^{90}$Sr的中子数为90-38=52,0.1 mol${\;}_{38}^{90}$Sr原子中含中子数为5.2NA,故B错误;
C.气体不一定在标况下,无法计算物质的量,故C错误;
D.由于溶液中铁离子部分水解,将0.1mol氯化铁溶于1L水中,所得溶液含有铁离子物质的量小于0.1mol,铁离子数目小于0.1NA个,故D错误.
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,阿伏加德罗常数是高考的“热点”,既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.要准确解答好这类题目,既要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,还要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 青砖(含Fe3O4)中的Fe2+可用浓盐酸溶解后,再加入适量高锰酸钾溶液进行检验 | |
| B. | 用0.1000 mol•L-1 NaOH溶液滴定20.00 mL未知浓度盐酸,接近终点时因滴速太快造成NaOH少许过量;此时若加入一定体积该盐酸后,继续用该NaOH溶液恰好滴定至终点,则测得的盐酸浓度将偏大 | |
| C. | 为了使实验现象明显,在做吸氧腐蚀实验时,不能用没有处理过的镀锌铁皮代替生铁 | |
| D. | 检查容量瓶瓶口是否漏水的方法是:往瓶内加入一定量水,塞好瓶塞.用食指摁住瓶塞,另一只手托住瓶底,把瓶倒转过来,观察瓶塞周围是否有水漏出即可 |
11.下列无色溶液中的离子能大量共存的是( )
| A. | K+、Na+、MnO4-、SO42- | B. | OH-、K+、HCO3-、SO32- | ||
| C. | H+、Mg2+、Cl-、Br- | D. | Al3+、NH4+、OH-、NO3- |
15.某无色溶液中可能含有①Na+②Ba2+③Cl-④Br -⑤S042-⑥SO32-中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
下列结论正确的是( )
| 步驟序号 | 操作步骤 | 现 象 |
| (1) | 用pH试纸检验 | 溶液的pH>7 |
| (2) | 向溶液中滴加氯水,再加人CC14、振荡、静置 | 下层呈橙色 |
| (3) | 向(2)所得水溶液中加人Ba(N03)2溶液和 稀 HNO3 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加人AgNO3溶液和稀HNO, | 有白色沉淀产生 |
| A. | 不能确定的离子是① | B. | 不能确定的离子是②③ | ||
| C. | 肯定含有的离子是①④⑥ | D. | 肯定没有的离子是②⑤ |
5.下列说法中正确的是( )
| A. | 高纯度的单晶硅可用于制造太阳能电池板和光导纤维 | |
| B. | 石油可以通过裂解、裂化等物理变化获得重要化工原料乙烯 | |
| C. | 鸡蛋清和淀粉溶液都属于胶体,遇到硫酸铜溶液可以发生胶体聚沉 | |
| D. | 植物油中由于含有碳碳双键,因此在空气中长时间放置容易氧化变质 |
12.下列关于厨房中的化学说法错误的是( )
| A. | 用热的碱水清除炊具上残留的油污比冷的碱水清除效果好 | |
| B. | 面粉和炒菜用的花生油的主要成分均为天然高分子化合物 | |
| C. | 炒菜用过的铁锅,经放置常出现红棕色斑迹,主要发生的是电化学腐蚀 | |
| D. | 早餐经常食用的豆浆和牛奶均属于胶体,且均含有丰富的蛋白质 |
9.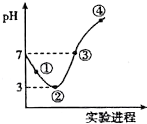 常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )
常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )
 常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )
常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )| A. | 用pH试纸测①处c(H+)约为②处c (H+)的两倍 | |
| B. | 可依据②处数据计算所溶解的n(Cl2) | |
| C. | ③处表示溶液中,c(Na+)=c(ClO-)+c(Cl-) | |
| D. | 曲线③④段有离子反应:HClO+OH-→ClO-+H2O |
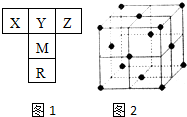 如图1是元素周期表的一部分.已知R的核电荷数小于36,气态氢化物沸点:MHn>YHn.
如图1是元素周期表的一部分.已知R的核电荷数小于36,气态氢化物沸点:MHn>YHn.